题目内容
16.常山胡柚闻名全国.胡柚适宜生长在PH为5.5~6.5的土壤环境中,对于pH为5.5以下的土壤,经过改良后也可种植.在胡柚生长过程中,为了防治“胡柚炭疽病”的发生,可适时喷洒农药波尔多液(熟石灰和硫酸铜的混合液).根据上述材料回答下列问题:(1)胡柚适宜生长在偏酸性(填“偏酸性”、“偏碱性”或“中性”)的土壤里;
(2)某块山地的土壤PH为5.5~4.8,欲种植胡柚,可采取的改良措施是撒适量熟石灰;
(3)从事胡柚种植的果农们在配制农药波尔多液时,均使用塑料桶或木桶,而不使用铁桶,其原因是(用化学方程示):Fe+CuSO4=FeSO4+Cu.
分析 (1)pH=7的溶液是中性溶液,pH<7的溶液是酸性溶液,pH>7的溶液为碱性溶液.
(2)酸性土壤中加入熟石灰可以使土壤酸性降低,有利于农作物的生长.
(3)铁在金属活动性顺序表中,位于铜的前面,能与硫酸铜发生置换反应.
解答 解:(1)胡柚适宜生长在pH为5.5~6.5的土壤环境中,呈酸性,故填:偏酸性;
(2)土壤pH为5.5~4.8,而胡柚适宜生长在pH为5.5~6.5的土壤环境中,故需要降低土壤的酸性,可以加入碱性物质,氢氧化钙具有碱性,可以用于改良酸性土壤,故填:撒适量熟石灰;
(3)铁能与波尔多液中的硫酸铜反应生成硫酸亚铁和铜,导致药效降低,故填:Fe+CuSO4=FeSO4+Cu.
点评 本题考查了溶液的酸碱性与pH的关系以及金属的有关知识,完成此题,可以依据已有的知识进行.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
4.现有银、铜、铁三种金属,某研究小组的同学为探究银、铜、铁的金属活动性顺序,设计了三个实验:I.将铁片浸入稀硫酸中,II.将银片浸入稀硫酸中,III.将铁片浸入硫酸铜溶液中.
(1)实验I的现象是,有气泡产生,溶液由无色逐渐变为浅绿色.反应的化学方程式为Fe+H2SO4=FeSO4+H2↑;反应产生的气体可用点燃的方法检验.
(2)上述三个实验还不能完全证明三种金属的活动性顺序,请你补充一个实验来达到实验目的(写出实验操作和现象)把铜片伸入硝酸银溶液中,铜片表面附着一层银白色固体.根据以上探究,三种金属的活动性由强到弱的顺序是铁、铜、银.
(3)将银、铜、铁的两种金属分别放入硫酸铜溶液中,即可验证这三种金属的活动性强弱.
(4)将铜片加热,铜片表面变黑.同学们设计如下实验证明此黑色物质是氧化铜.
写出该气体还原氧化铜的方程式CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
(1)实验I的现象是,有气泡产生,溶液由无色逐渐变为浅绿色.反应的化学方程式为Fe+H2SO4=FeSO4+H2↑;反应产生的气体可用点燃的方法检验.
(2)上述三个实验还不能完全证明三种金属的活动性顺序,请你补充一个实验来达到实验目的(写出实验操作和现象)把铜片伸入硝酸银溶液中,铜片表面附着一层银白色固体.根据以上探究,三种金属的活动性由强到弱的顺序是铁、铜、银.
(3)将银、铜、铁的两种金属分别放入硫酸铜溶液中,即可验证这三种金属的活动性强弱.
(4)将铜片加热,铜片表面变黑.同学们设计如下实验证明此黑色物质是氧化铜.
| ①实验操作 | ②实验现象 |
| 剪下一片变黑的铜片,放入试管中, 通入足量的一氧化碳气体 | 铜片表面的黑色物质全部消失,露出红色的铜,将生成的气体通入澄清石灰水,石灰水变浑浊 |
6.在制取CO2的实验中,小科发现质量相同而粗细不同的大理石与盐酸反应,CO2的产生速度细的比粗的快得多.经思考后,小科设计了如下实验(每次实验均用1g大理石,20mL盐酸)
(1)为了比较反应速度,设计如图一所示装置,其中量筒的作用是通过观察单位时间内排入量筒中水的体积来判断反应速率;
(2)实验中CO2体积随时间的变化关系如图二所示,请将实验2中CO2体积随时间变化的曲线画在图二中.
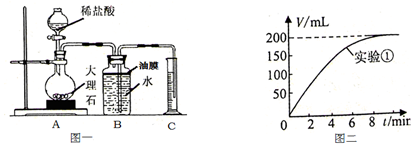
(3)已知20℃该气压下CO2气体密度约1.98g/L,求大理石中CaCO3的质量分数?
| 实验序号 | 温度(℃) | 大理石颗粒 | 盐酸质量分数(%) | 实验目的 |
| 1 | 20 | 粗 | 5 | 探究大理石和盐酸的反应速度与石灰石颗粒大小的关系 |
| 2 | 20 | 细 | 5 |
(2)实验中CO2体积随时间的变化关系如图二所示,请将实验2中CO2体积随时间变化的曲线画在图二中.

(3)已知20℃该气压下CO2气体密度约1.98g/L,求大理石中CaCO3的质量分数?
 某化学兴趣小组为了测定镁铜合金中镁的质量分数,取出2克合金样品,每次加入稀硫酸10克,共加入稀硫酸4次,充分反应后,过滤、洗涤、干燥、称重,得到的实验数据如图所示:
某化学兴趣小组为了测定镁铜合金中镁的质量分数,取出2克合金样品,每次加入稀硫酸10克,共加入稀硫酸4次,充分反应后,过滤、洗涤、干燥、称重,得到的实验数据如图所示: