题目内容
3.如图是几种常见物质的转化关系,其中A是单质,甲覆盖了地球表面的约71%,B是最清洁的能源,试分析回答下列问题: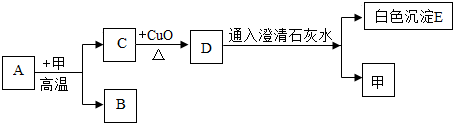
(1)写出两种物质的化学式:CCO,ECaCO3;
(2)A和甲反应的化学方程式:C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2.
分析 因为澄清石灰水变浑浊,因此D为二氧化碳、E是碳酸钙,甲覆盖了地球表面的约71%,因此甲是水;B是最清洁的能源,因此B是氢气,C能够和氧化铜反应产生二氧化碳,则C是一氧化碳,因此A是碳,据此分析.
解答 解:因为澄清石灰水变浑浊,因此D为二氧化碳、E是碳酸钙;甲覆盖了地球表面的约71%,因此甲是水;B是最清洁的能源,因此B是氢气,C能够和氧化铜反应产生二氧化碳,则C是一氧化碳,因此A是碳,因此:
(1)C是一氧化碳,E是碳酸钙,故化学式分别为:CO;CaCO3;
(2)碳和水在高温条件下生成一氧化碳和氢气,故反应的方程式为:C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2.
点评 本题考查了常见物质的推断,在解此类题时,首先将题中有特征的物质推出,然后依据推出的物质再去推导其他的物质,最后进行验证即可.

练习册系列答案
 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
13.下列设计方案探究目的不能实现的是( )


| A. | 甲可探究可燃物的燃烧是否需要与氧气接触 | |
| B. | 甲可探究可燃物的燃烧是否需要达到一定的温度 | |
| C. | 乙中①③对比可探究铁的锈蚀条件与氧气是否有关 | |
| D. | 乙中①②③对比可探究铁的锈蚀条件与氧气和水是否有关 |
14.已知氢氧化钾(KOH)可溶于水,其化学性质与氢氧化钠相似,下列对氢氧化钾的化学性质的说法中错误的是( )
| A. | 能使紫色石蕊溶液变红 | B. | 能使无色酚酞溶液变红 | ||
| C. | 能与稀盐酸反应 | D. | 能与二氧化碳反应 |
18.下列说法中,正确的是( )
| A. | 煤炉上放一壶水可以防止CO中毒 | |
| B. | 金刚石、石墨都是由碳原子构成的,所以都很坚硬 | |
| C. | 用活性碳可以除去水中的色素和臭味 | |
| D. | CO、CO2都能使澄清石灰的石灰水变浑浊 |
8.现有铜与另一种金属的混合物粉末,另一种金属可能是镁、铁、锌中的一种,现欲测定其组成.取该混合物粉末8.0g放入烧杯中,将140.0g 14.0%的稀硫酸分四次加入该烧杯中,充分反应后,测得剩余固体质量数据记录如下:
求:
(1)该混合物粉末中铜的质量分数52.5%;
(2)若参加反应的金属为R,请写出R与稀硫酸反应的化学方程式R+H2SO4═RSO4+H2↑;
(3)设金属R的相对原子质量为X,根据已知条件列出求解(X)的比例式$\frac{X}{98}=\frac{1.2g}{4.9g}$;
(4)如果将第三次加入硫酸充分反应后的溶液蒸发掉8.3g水,且无晶体析出,则所得溶液中溶质的质量分数为18.0%.
| 次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸的质量/g | 35.0 | 35.0 | 35.0 | 35.0 |
| 剩余固体的质量/g | 6.8 | 5.6 | 4.4 | 4.2 |
(1)该混合物粉末中铜的质量分数52.5%;
(2)若参加反应的金属为R,请写出R与稀硫酸反应的化学方程式R+H2SO4═RSO4+H2↑;
(3)设金属R的相对原子质量为X,根据已知条件列出求解(X)的比例式$\frac{X}{98}=\frac{1.2g}{4.9g}$;
(4)如果将第三次加入硫酸充分反应后的溶液蒸发掉8.3g水,且无晶体析出,则所得溶液中溶质的质量分数为18.0%.
12.甲同学欲通过实验证明“二氧化锰是过氧化氢分解的催化剂”之一命题.该同学设计并完成了下表所示的探究实验:
(1)请你帮甲同学填写上表中未填完的空格;
(2)在甲的探究实验中,实验一和实验二起的作用是对比;
(3)乙同学认为仅由上述实验还不能完全得出表内“总结”,乙同学补充设计了两个方面的探究实验,最终完成了对“命题”的实验证明.
第一方面的实验操作中包含了两次称量,其目的是:比较MnO2在过氧化氢分解前后的质量;
第二方面的实验是利用“实验三”反应后试管内的剩余物继续实验.接下来的实验操作、现象和结论是:向剩余的固体中重新加人过氧化氢溶液,伸入带火星的木条,有大量气泡产生,木条复燃,说明MnO2仍然能加快过氧化氢的分解..
| 实验操作 | 实验现象 | 实验结论或总结 | ||
| 结论 | 总结 | |||
| 实验一 | 取5mL 5%的过氧化氢溶液于试管中,伸入带火星的木条 | 有气泡产生,木条不复燃 | 过氧化氢分解产生氧气,但是反应慢.反应的化学方程式为2H2O2=2H2O+O2↑ | 二氧化锰是过氧化氢分解的催化剂 |
| 实验二 | 向盛水的试管中加入二氧化锰,伸入带火星的木条 | 没有明显现象 | 二氧化锰加入水中不产生氧气 | |
| 实验三 | 向盛有5mL5%的过氧化氢溶液的试管中加入二氧化锰,伸入带火星的木条 | 大量气泡产生,带火星的木条迅速复燃 | 二氧化锰能加快过氧化氢的分解 | |
(2)在甲的探究实验中,实验一和实验二起的作用是对比;
(3)乙同学认为仅由上述实验还不能完全得出表内“总结”,乙同学补充设计了两个方面的探究实验,最终完成了对“命题”的实验证明.
第一方面的实验操作中包含了两次称量,其目的是:比较MnO2在过氧化氢分解前后的质量;
第二方面的实验是利用“实验三”反应后试管内的剩余物继续实验.接下来的实验操作、现象和结论是:向剩余的固体中重新加人过氧化氢溶液,伸入带火星的木条,有大量气泡产生,木条复燃,说明MnO2仍然能加快过氧化氢的分解..
13.下列四个图象中,能正确反映对应变化关系的是( )
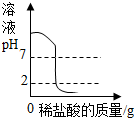 | 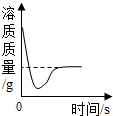 | 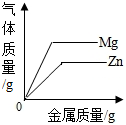 | 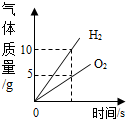 |
| A.向一定量的氢氧化钠溶液中逐滴加入pH=2的稀盐酸至过量 | B.某温度时,向一定量的饱和石灰水中加入少量生石灰 | C.向两份完全相同的稀盐酸中分别加入足量的锌粉、镁粉 | D.将水通电一段时间 |
| A. | A | B. | B | C. | C | D. | D |
