题目内容
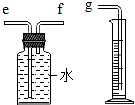
下列实验操作中错误的是 ( )
( )
A.
点燃酒精灯 B.
滴加溶液 C.
量筒读数 D.
放置滴管
【考点】加热器皿-酒精灯;测量容器-量筒;液体药品的取用.
【专题】化学学习中的实验思想;常见仪器及化学实验基本操作.
【分析】A、根据酒精灯的使用方法分析.
B、根据胶头滴管的使用方法分析.
C、根据量取液体体积的注意事项分析;
D、根据胶头滴管的使用方法分析.
【解答】解:A、点燃酒精灯应用火柴点燃,图中操作正确;
B、使用胶头滴管滴加少量液体时,注意胶头滴管的位置是不伸入到试管内或接触试管内壁.应垂直悬空在试管口上方滴加液体,防止污染胶头滴管,图中操作正确.
C、用量筒量取液体时,视线没与液体的凹液面最低处保持水平,图中操作正确.
D、吸取液体后的胶头滴管不能平放或倒置,以防试剂倒流腐蚀橡胶帽,图示操作错误.
故选:D.
【点评】本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键.

 考前必练系列答案
考前必练系列答案向烧杯中逐滴加入X溶液至过量(图甲),生成沉淀或气体的质量(纵坐标)与加入X溶液的质量(横坐标)关系不符合图乙的是( )
| 烧杯中的物质 | X溶液 | |
| A | 稀硫酸 | 氯化钡溶液 |
| B | 稀硫酸和硫酸铜溶液 | 氢氧化钠溶液 |
| C | 氯化钙溶液 | 碳酸钠溶液 |
| D | 碳酸氢钠溶液 | 稀盐酸 |
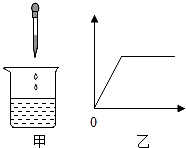
A.A B.B C.C D.D
甲同学为了区别氢氧化钠和氢氧化钙溶液,设计了如图所示的四组实验方案.
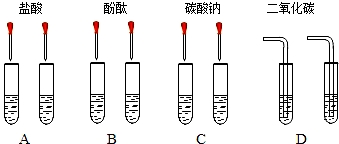
(1)其中能达到实验目的是
(2)在C组实验中发生的化学方程式为
(3)实验结束后,甲同学将A、C组四支试管中的溶液倒入同一容器中,看到溶液变浑浊,该现象说明有 物质生成(填化学式),滴入酚酞后溶液呈红色.
(4)滴入酚酞后溶液呈红色,说明溶液呈碱性.使溶液呈碱性的物质是什么呢?甲同学进一步推测:溶液中呈碱性的物质可能是碳酸钠、氢氧化钙和 三种物质中的一种,或是三种物质两两混合组成的混合物.
(5)为了验证推测,甲同学查阅资料,获悉氯化钡溶液呈中性,并设计如下实验加以验证.请根据要求完成下列空白:
| 实验内容 | 预测现象 | 结论 |
| 取少量容器中的上层溶液于试管中,加入过量的氯化钡溶液,静置 | ①若有白色沉淀,溶液呈无色 | 物质是碳酸钠 |
| ②若无沉淀生成,溶液呈红色 | 物质是氢氧化钙 | |
| ③若有白色沉淀,溶液呈红色 |
|
(6)乙同学认为甲同学第②步验证的结论不严密,原因是 .
“五一”假期,小兵对“锌与硫酸反应快慢的影响因素”进行了探究.
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】a.可能与硫酸的质量分数有关;b.可能与锌的形状有关.
【设计并实验】小兵用不同质量分数的硫酸和不同形状的锌进行如下实验.
| 实验编号 | 硫酸的质量分数(均取20mL) | 锌的形状(均取1g) | 氢气的体积(mL)(均收集3分钟) |
| ① | 30% | 锌粒 | 31.7 |
| ② | 20% | 锌片 | 50.9 |
| ③ | 20% | 锌粒 | 61.7 |
| ④ | 30% | 锌片 | 79.9 |
(1)写出稀硫酸与锌反应的化学方程式 .
(2)小兵用如图装置收集并测量氢气的体积,其中量筒的作用是 ,
氢气应从 (填e或f或g)管通入.
(3)若用该收集CO2,并测量生成的CO2气体的体积,其中在水面上放一层植物油目的是 ;
【收集证据】(4)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是 .
【得出结论】(5)结论是
【评价与反思】(注意:若答对(5)(6)两小题奖励4分,化学试卷总分不超过60分)
(6)下表是小兵第①组实验的详细数据.
| 时段(均为1分钟) | 第1分钟 | 第2分钟 | 第3分钟 | 第4分钟 | 第5分钟 | 第6分钟 |
| H2的体积 | 3.1mL | 16.7mL | 11.9mL | 9.6mL | 7.6mL | 6.0mL |
请描述锌与硫酸反应的快慢的变化并解释原因 .
(7)锌与硫酸反应的快慢可能还受哪些因素影响?设计实验验证. .