题目内容
9.化学与生活息息相关,请你用化学知识回答以下生活中的问题.(1)区别棉纤维、羊毛纤维和合成纤维的最简单方法是做燃烧实验.
(2)若装白磷的储罐起火,可以用水灭火,也可以用沙土填埋灭火.其中用沙土填埋灭火的原理是隔绝氧气.
(3)铝制品抗腐蚀性能很好,原理是4Al+3O2═2Al2O3(用化学方程式表示).
分析 (1)羊毛纤维的主要成分是蛋白质,蛋白质燃烧时能产生烧焦羽毛的气味,据此进行分析解答.
(2)根据灭火原理:①清除或隔离可燃物,②隔绝氧气或空气,③使温度降到可燃物的着火点以下,据此结合灭火方法进行分析解答.
(3)铝具有良好的抗腐蚀性能,是因为铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,据此写出反应的化学方程式即可.
解答 解:(1)羊毛纤维的主要成分是蛋白质,蛋白质燃烧时能产生烧焦羽毛的气味,棉纤维没有,合成纤维燃烧会产生特殊气味,区别棉纤维、羊毛纤维和合成纤维的最简单方法是做燃烧实验.
(2)若装白磷的储罐起火,可以用水灭火,也可以用沙土填埋灭火.其中用沙土填埋灭火的原理是隔绝氧气.
(3)铝具有良好的抗腐蚀性能,是因为铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,反应的化学方程式为:4Al+3O2═2Al2O3.
故答案为:(1)燃烧;(2)隔绝氧气;(3)4Al+3O2═2Al2O3.
点评 本题难度不大,掌握棉纤维、羊毛纤维和合成纤维的鉴别方法、灭火的原理、金属的化学性质等是正确解答本题的关键.

练习册系列答案
相关题目
10.如图是A、B、C三种固体溶质(均不含结晶水)的溶解度曲线,根据图示,下列说法不正确的是
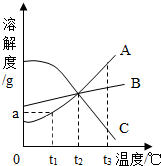

| A. | t1℃时,取50gA的饱和溶液,将温度升高到t2℃,此时溶液中A的质量分数不变(假设升温时,溶剂没有损失) | |
| B. | t1℃,将A、B、C各ag放入100g水中,充分搅拌,所得溶液溶质质量分数均相等 | |
| C. | t3℃时,取相同质量的A、B、C三种饱和溶液降温到t1℃,析出晶体最多的是A | |
| D. | 从A与少量C的混合物中提纯A,可用蒸发结晶的方法 |
17.下列既不属于描述物质的化学性质,也不属于化学变化的叙述是( )
| A. | 酒精具有挥发性;碘酒洒在衣服上可用酒精擦洗干净 | |
| B. | 硫酸具有酸的通性;浓硫酸能使木材炭化 | |
| C. | 氢气可以还原氧化铁;铁丝在氧气中燃烧可生成黑色固体物质 | |
| D. | 二氧化硫具有刺激性气味;块状生石灰在空气中会变成粉末 |
4.生活中常用来软化水的方法是( )
| A. | 过滤 | B. | 加热煮沸 | C. | 蒸馏 | D. | 蒸发 |
14.下列实验操作中,正确的是( )
| A. | 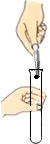 取块状固体 | B. |  闻气体气味 | C. | 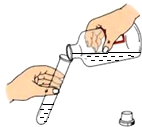 倾倒液体 | D. | 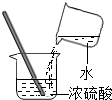 稀释浓硫酸 稀释浓硫酸 |
1.有失去标签的三瓶无色溶液,分别是稀盐酸、氯化钠溶液(中性)和氢氧化钠溶液.欲设计实验对其进行鉴别.
(1)小明选择紫色石蕊溶液对其鉴别,请在以下表格中填写相应的现象
(2)如果实验室没有石蕊溶液,可以用无色酚酞先鉴别出三种溶液中的氢氧化钠溶液,
剩下的两种溶液,小明提议可以用大理石或石灰石进行区分,请写出相关的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑.
(3)盐酸有多种用途,可以用它来除去铁锈(主要成分是氧化铁),请用化学方程式表示盐酸除锈的原理Fe2O3+6HCl═2FeCl3+3H2O.
(1)小明选择紫色石蕊溶液对其鉴别,请在以下表格中填写相应的现象
| 实验操作 | 实验现象 | 实验结论 |
| 分别取少量待测液与三支试管中,分别滴加紫色石蕊试液 | ||
剩下的两种溶液,小明提议可以用大理石或石灰石进行区分,请写出相关的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑.
(3)盐酸有多种用途,可以用它来除去铁锈(主要成分是氧化铁),请用化学方程式表示盐酸除锈的原理Fe2O3+6HCl═2FeCl3+3H2O.
18.通过下列各组对比实验,能得到相应结论的是( )
| 实验方案 | 实验结论 | ||
| 实验? | 实验? | ||
| A | 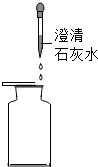 空气 | 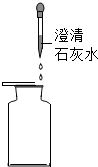 人呼出的气体 | 人呼出的气体全部是CO2 |
| B | 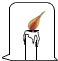 | 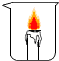 | 燃烧需要可燃物的温度达到着火点 |
| C | 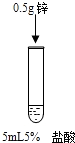 | 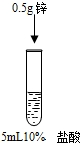 | 盐酸的浓度对反应剧烈程度有影响 |
| D | 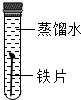 | 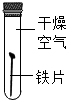 | 铁生锈需要氧气和水 |
| A. | A | B. | B | C. | C | D. | D |
19.下列物质间的转化,不能通过一步反应实现的是( )
| A. | CuO→CuCl2 | B. | KMnO4→MnO2 | C. | Al→H2 | D. | Fe→FeCl3 |