题目内容
现将含ZnO 50%(其他成分不含锌)的矿石10t与一定量的赤铜、木炭粉混合加热到约800℃,反应完全后可得到含锌65%的锌铜多少吨?(列式计算,计算结果保留1位小数)
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:氧化锌与木炭在高温下反应生成锌和二氧化碳;由矿石的质量、氧化锌的质量分数,由反应的化学方程式计算出生成锌的质量;进而可计算出含锌65%的锌铜的质量.
解答:解;设生成锌的质量为x
C+2ZnO
2Zn+CO2↑
162 130
10t×50% x
=
x≈4.0t
反应完全后可得到含锌65%的锌铜4.0t÷65%≈6.2t.
答:反应完全后可得到含锌65%的锌铜的质量为6.2t.
C+2ZnO
| ||
162 130
10t×50% x
| 162 |
| 130 |
| 10t×50% |
| x |
反应完全后可得到含锌65%的锌铜4.0t÷65%≈6.2t.
答:反应完全后可得到含锌65%的锌铜的质量为6.2t.
点评:本题难度不大,考查含杂质物质的化学方程式的计算,注意代入方程式计算的必须是纯物质的质量是正确解答此类题的关键.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
将铁、镁、铝三种金属分别放入稀盐酸中,充分反应后,放出的气体质量相同,其原因可能是( )
| A、放入铁、镁、铝的质量相同,跟足量的稀盐酸反应 |
| B、放入铁、镁、铝的质量比是28:12:9跟足量的稀盐酸反应 |
| C、放入铁、镁、铝的质量比是56:24:27,跟足量的稀盐酸反应 |
| D、放入铁、镁、铝均为过量,跟三种金属反应的稀盐酸的质量相同,质量分数也相同 |
关于酸和碱的性质说法正确的是( )
| A、用盐酸不能洗掉敞口盛放石灰水试剂瓶内壁的白色固体 |
| B、用稀硫酸可洗掉试管里残存的红褐色氢氧化铁 |
| C、酸具有一些相似的化学性质,原因是它们都能与金属反应有氢气产生 |
| D、碱具有一些相似的化学性质,原因是它们都能与空气中的二氧化碳反应 |
 分别表示A和B两种不同原子,下图能表示“2A2”的是( )
分别表示A和B两种不同原子,下图能表示“2A2”的是( )A、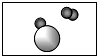 |
B、 |
C、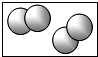 |
D、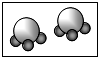 |
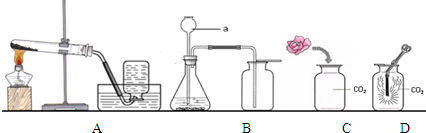
 A、B、C、D、E、F分别是稀硫酸、氢氧化钠溶液、水、二氧化碳、氧化铜和木炭中的一种物质,其中C在常温下是气体,用圆和五边形表示这六种物质.它们之间的转化关系如图所示(图中“→”表示一种物质能转化为另一种物质,“-”表示两端的物质能发生反应,图中已略去部分物质).(已知木炭和水蒸气在高温下可以反应生成一氧化碳和氢气)
A、B、C、D、E、F分别是稀硫酸、氢氧化钠溶液、水、二氧化碳、氧化铜和木炭中的一种物质,其中C在常温下是气体,用圆和五边形表示这六种物质.它们之间的转化关系如图所示(图中“→”表示一种物质能转化为另一种物质,“-”表示两端的物质能发生反应,图中已略去部分物质).(已知木炭和水蒸气在高温下可以反应生成一氧化碳和氢气)