题目内容
18. “更高、更快、更强”的奥运精神在化学学习中有所体现.请分析题意,按要求回答问题:
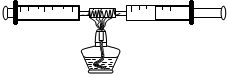
“更高、更快、更强”的奥运精神在化学学习中有所体现.请分析题意,按要求回答问题:(1)写出如图实验一中“更高”的化学方程式:CO2+2NaOH═Na2CO3+H2O.
由此实验你认为实验室除去混合气体中的二氧化碳气体杂质的最佳试剂是氢氧化钠溶液;理由是氢氧化钙微溶于水,氢氧化钠溶于水,等量的水中溶解的氢氧化钠多,吸收效果好.
(2)写出如图实验二中“更快”的化学方程式:Mg+2HCl═MgCl2+H2↑.造成两者反应速度快慢不同的因素是金属活动性不同
(3)“更强”,辩论见风采.某学校化学兴趣小组的同学准备了一场辩论赛.辩论主题是“1+1等于不等于2.”甲方认为:1+1等于2.乙方认为:1+1不等于2.
请根据溶液的相关知识判断.
①如果你认为甲方正确,请举一例溶液中溶液质量等于溶质和溶剂质量之和;
②如果你认为乙方正确,请举一例两种不同液体互溶,得到的液体体积小于两种液体体积.
分析 (1)二氧化碳与石灰水反应生成碳酸钙沉淀和水,氢氧化钠溶液能与二氧化碳反应生成碳酸钠和水,由于氢氧化钠易溶于水,氢氧化钙微溶于水,氢氧化钠溶液中吸收的二氧化碳比较多,盛氢氧化钠溶液的水槽中试管液面上升高.
(2)在金属活动性顺序中,金属的活动性越强,反应速率越快,进行分析解答.
(3)①根据溶液是由溶质和溶剂组成的,继续分析解答.
②根据分子间有间隔,进行分析解答.
解答 解:(1)二氧化碳与石灰水反应生成碳酸钙沉淀和水,氢氧化钠溶液能与二氧化碳反应生成碳酸钠和水,由于氢氧化钠易溶于水,氢氧化钙微溶于水,氢氧化钠溶液中吸收的二氧化碳比较多,盛氢氧化钠溶液的水槽中试管液面上升高,反应的化学方程式为:CO2+2NaOH═Na2CO3+H2O.
由此实验你认为实验室除去混合气体中的二氧化碳气体杂质的最佳试剂是氢氧化钠溶液,原因是氢氧化钙微溶于水,氢氧化钠溶于水,等量的水中溶解的氢氧化钠多,吸收效果好.
(2)在金属活动性顺序中,镁排在铁的前面,反应速度别铁快,镁与稀盐酸反应生成氯化镁和氢气,反应的化学方程式为:Mg+2HCl═MgCl2+H2↑.
造成两者反应速度快慢不同的因素是金属活动性不同.
(3)①溶液是由溶质和溶剂组成的,溶液的质量等于溶质的质量和溶剂的质量之和.
②分子间有间隔,两种不同的分子会互相占据分子之间的间隔,故两种不同液体互溶,得到的液体体积小于两种液体体积.
故答案为:(1)CO2+2NaOH═Na2CO3+H2O;氢氧化钠溶液;氢氧化钙微溶于水,氢氧化钠溶于水,等量的水中溶解的氢氧化钠多,吸收效果好;
(2)Mg+2HCl═MgCl2+H2↑;金属活动性不同;
(3)①溶液中溶液质量等于溶质和溶剂质量之和;②两种不同液体互溶,得到的液体体积小于两种液体体积.
点评 本题难度不大,熟练掌握碱的化学性质、金属的化学性质、溶液的特征等是正确解答本题的关键.

 备战中考寒假系列答案
备战中考寒假系列答案| A. | Zn+H2SO4(稀)=ZnSO4+H2↑ | |
| B. | 焦炭与水蒸气反应:C+H2O(气)$\frac{\underline{\;高温\;}}{\;}$H2+CO | |
| C. | 太阳光分解水:2H2O $\frac{\underline{\;\;\;TiO_{2}\;\;\;}}{太阳光}$ 2H2↑+O2↑ | |
| D. | 电解水:2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑ |
| A. | 盐酸 | B. | 氯化铜溶液 | C. | 石蕊试液 | D. | 二氧化碳 |
| A. | 使用蜡烛时不慎使书本着火,用湿布盖灭 | |
| B. | 厨房燃气管漏气,立即打开排气扇电源排气 | |
| C. | 实验时,把没有用完的白磷丢进垃圾筐里 | |
| D. | 高楼着火,乘电梯逃生 |
| A. | H2SO4 | B. | NaCl | C. | KNO3 | D. | Ca(OH)2 |

 如图所示是某同学测定空气中氧气含量的装置.玻璃管中装的是细铜丝.
如图所示是某同学测定空气中氧气含量的装置.玻璃管中装的是细铜丝.