题目内容
14.某化学兴趣小组的同学对能制氧气的呼吸面具进行研究.【查阅资料】
(1)呼吸面具中制取氧气的主要原料是固体过氧化钠(Na2O2).过氧化钠分别能和二氧化碳、水反应,都生成氧气,反应的化学方程式为:
①2Na2O2+2H2O═4NaOH+O2↑
②2Na2O2+2CO2═2Na2CO3+O2
(2)氯化钙溶液呈中性;碳酸钠溶液呈碱性;
氯化钙溶液与碳酸钠溶液混合后发生如下反应:Na2CO3+CaCl2═CaCO3↓+2NaCl.
同学们对用过一段时间后的面具中的固体成分产生兴趣.
【猜想与假设】
固体可能为:①Na2CO3;②NaOH和Na2CO3;③Na2O2和Na2CO3;④Na2O2和NaOH.
为了确定用过一段时间后呼吸面具中的成分,该小组的同学在老师的指导下进行了以下的探究.
【进行实验】
实验Ⅰ:取少量固体放入试管中,加足量水,看到产生气泡,证明固体中有Na2O2.
实验Ⅱ:取少量固体放入试管中,滴加足量的稀盐酸,看到产生气泡,则证明固体中含有Na2CO3.
实验Ⅲ:取少量固体放入试管中,加足量水,再滴加足量的氯化钙溶液后,过滤.向滤液中加入酚酞试液,若溶液变成红色,则证明固体中含有NaOH.
【反思与评价】
通过上述实验,有些同学认为其中有些不妥的结论.
(1)有些同学认为通过实验Ⅱ并不能确定固体中含有Na2CO3.如何改进此实验?取少量固体放入试管中,滴加澄清石灰水,澄清石灰水变浑浊,说明固体中含有碳酸钠.
加热
(2)还有些同学认为通过实验Ⅲ也不能证明固体中一定含有NaOH.其原因是:过氧化钠和水反应生成氢氧化钠,氢氧化钠溶液能使酚酞试液变红色.
(3)某实验小组为研究碳酸钠和碳酸氢钠混合物的组成做了以下实验:充分加热10.0g样品至恒重,剩余固体质量为6.9g.(2NaHCO3═Na2CO3+CO2+H2O)
查阅资料已知:碳酸氢钠受热易分解生成碳酸钠、水和二氧化碳;碳酸钠受热不易分解.
计算:(1)生成二氧化碳的质量2.2g.
(2)原混合物中碳酸钠的质量分数.
分析 【猜想与假设】
固体可能为:①Na2CO3;②NaOH和Na2CO3;③Na2O2和Na2CO3;④Na2O2和NaOH.
【进行实验】
根据实验现象可以判断实验结论,根据实验结论可以判断实验现象;
显碱性溶液能使酚酞试液变红色;
【反思与评价】
碳酸钠能和氢氧化钙反应生成白色沉淀碳酸钙和氢氧化钠;
根据反应的化学方程式和提供的数据可以进行相关方面的计算.
解答 解:【猜想与假设】
固体可能为:①Na2CO3;②NaOH和Na2CO3;③Na2O2和Na2CO3;④Na2O2和NaOH.
故填:Na2O2和NaOH.
【进行实验】
实验Ⅰ:取少量固体放入试管中,加足量水,看到产生气泡,证明固体中有Na2O2.
故填:产生气泡.
实验Ⅱ:取少量固体放入试管中,滴加足量的稀盐酸,看到产生气泡,则证明固体中含有Na2CO3.
故填:产生气泡.
实验Ⅲ:取少量固体放入试管中,加足量水,再滴加足量的氯化钙溶液后,过滤.向滤液中加入酚酞试液,若溶液变成红色,则证明固体中含有NaOH.
故填:红色.
【反思与评价】
(1)有些同学认为通过实验Ⅱ并不能确定固体中含有Na2CO3,改进此实验为:取少量固体放入试管中,滴加澄清石灰水,澄清石灰水变浑浊,说明固体中含有碳酸钠.
故填:取少量固体放入试管中,滴加澄清石灰水,澄清石灰水变浑浊,说明固体中含有碳酸钠.
(2)通过实验Ⅲ也不能证明固体中一定含有NaOH,其原因是:过氧化钠和水反应生成氢氧化钠,氢氧化钠溶液能使酚酞试液变红色.
故填:过氧化钠和水反应生成氢氧化钠,氢氧化钠溶液能使酚酞试液变红色.
(3)设碳酸氢钠质量为x,
反应生成水和二氧化碳质量为:10.0g-6.9g=3.1g,
生成二氧化碳质量为:3.1g×$\frac{44}{62}$=2.2g,
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,
168 62
x 3.1g
$\frac{168}{x}$=$\frac{62}{3.1g}$,
x=8.4g,
原混合物中碳酸钠的质量分数为:$\frac{10.0g-8.4g}{10.0g}$×100%=16%,
答:原混合物中碳酸钠的质量分数为16%.
故填:2.2g.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

 阅读快车系列答案
阅读快车系列答案| A. | ①③④ | B. | ①④⑤ | C. | ②③④ | D. | ②③⑤ |
| A. | Fe2+和Na+ | B. | Fe3+和Na+ | C. | Cu2+和Ag+ | D. | 只有Na+ |
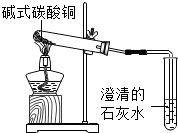 铜器长期暴露在空气中会生成铜绿(俗称铜锈).铜锈的主要成分是碱式碳酸铜,碱式碳酸铜不稳定,受热分解成黑色固体物质、无色气体和水.这种黑色固体和无色液体的成分是什么呢?
铜器长期暴露在空气中会生成铜绿(俗称铜锈).铜锈的主要成分是碱式碳酸铜,碱式碳酸铜不稳定,受热分解成黑色固体物质、无色气体和水.这种黑色固体和无色液体的成分是什么呢? 如图是硫酸试剂瓶标签上的内容.为了检验某钢材样品中铁的含量,需要把浓硫酸稀释为稀硫酸.根据计算回答下列问题:
如图是硫酸试剂瓶标签上的内容.为了检验某钢材样品中铁的含量,需要把浓硫酸稀释为稀硫酸.根据计算回答下列问题: