题目内容
12.将等质量、等质量分数的氢氧化钠溶液和硫酸溶液混合,混合后的溶液不能与下列物质发生反应的是( )| A. | CuSO4 | B. | FeCl3 | C. | HCl | D. | Fe |
分析 根据氢氧化钠与硫酸反应的化学方程式,判断完全反应后剩余的是哪一种溶液,结合酸或碱的化学性质,进行分析判断.
解答 解:等质量、等质量分数的氢氧化钠溶液和硫酸溶液混合后,硫酸与氢氧化钠溶液中所含溶质的质量相等.
反应中消耗硫酸与氢氧化钠的质量比关系如下:
H2SO4+2NaOH═Na2SO4+2H2O
98 80
可知,98份质量的硫酸与80份质量的氢氧化钠恰好完全反应,则等质量、等质量分数的氢氧化钠溶液和硫酸溶液混合,氢氧化钠有剩余.
A、氢氧化钠能与硫酸铜反应生成氢氧化铜沉淀和硫酸钠,故选项错误.
B、氢氧化钠能与FeCl3反应生成氢氧化铁沉淀和氯化钠,故选项错误.
C、氢氧化钠能与盐酸反应生成氯化钠和水,故选项错误.
D、氢氧化钠能与铁不反应,故选项正确.
故选:D.
点评 本题难度不大,掌握中和反应应用,根据化学方程式的计算判断出反应后剩余的物质是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.下列化学用语正确的是( )
| A. | N5:5个氮原子 | |
| B. | 2O2:2个氧分子 | |
| C. | Zn2+:正二价的锌元素 | |
| D. | 铝与盐酸的反应:Al+2HCl=AlCl2+H2↑ |
15.下列物质由原子构成的是( )
| A. | 氧化铜 | B. | 氧气 | C. | 氯化钠 | D. | 金刚石 |
12.图中的 A~H 是初中化学常见的化合物,且分别是由 H、O、S、Na、Ca、Cu 中的两种或三种元素组成的.其中 B、E 是氧化物,C、F、H 为相同类别的 化合物,F 易溶于水并放出大量的热,G 的溶液呈蓝色,图中“-”表示两端的物 质间能发生化学反应;“→”表示物质间存在转化关系,部分反应物、生成物或反 应条件已略去.下列说法错误的是( )
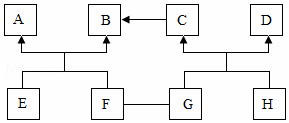

| A. | G 的化学式为 CuSO4 | B. | E 和 F 发生的是复分解反应 | ||
| C. | C B 可能是酸碱中和反应 | D. | A 和 D 的物质类别相同 |
17.实验小组同学用完全相同的4个充满二氧化碳的软塑料瓶验证二氧化碳的化学性质.
已知:通常状况下,1体积的水约能溶解1体积二氧化碳.
(1)实验1中发生反应的化学方程式为CO2+H2O=H2CO3;实验2中发生反应的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O.
(2)上述4个实验中,验证了CO2能与NaOH反应的实验有1和3;2和3;4(填序号).
(3)请判断实验1能否证明二氧化碳与水反应?并说明理由不能;因为通常情况下,1体积水能溶解1体积二氧化碳,瓶子变瘪可能只是由二氧化碳溶于水导致的.
| 实验 | 操作 | 现象 |
| 1 | 向瓶①内倒入1/3体积水,迅速拧紧瓶盖,振荡 | 瓶子均变瘪,变瘪程度依次为①<②<④<③ |
| 2 | 向瓶②内倒入1/3体积饱和石灰水,迅速拧紧瓶盖,振荡 | |
| 3 | 向瓶③内倒入1/3体积5%氢氧化钠溶液,迅速拧紧瓶盖,振荡 | |
| 4 | 向瓶④内倒入1/10体积氢氧化钠固体,迅速拧紧瓶盖,振荡 |
(1)实验1中发生反应的化学方程式为CO2+H2O=H2CO3;实验2中发生反应的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O.
(2)上述4个实验中,验证了CO2能与NaOH反应的实验有1和3;2和3;4(填序号).
(3)请判断实验1能否证明二氧化碳与水反应?并说明理由不能;因为通常情况下,1体积水能溶解1体积二氧化碳,瓶子变瘪可能只是由二氧化碳溶于水导致的.
4.下列粒子结构示意图中表示阳离子的是( )
| A. |  | B. |  | C. |  | D. |  |
1.防火安全教育是学校教育的一项必修课,下列有关燃烧与灭火的说法错误的是( )
| A. | 油锅着火用锅盖盖灭-隔绝空气 | |
| B. | 森林灭火时,建立隔离带-隔绝可燃物 | |
| C. | 用嘴吹灭洒落在实验桌上燃着的酒精-降低着火点 | |
| D. | 家具起火,用水扑灭-降低可燃物的温度至着火点以下 |
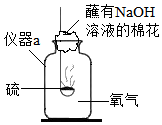 某同学对硫在氧气中燃烧的实验作了如图所示的改进.
某同学对硫在氧气中燃烧的实验作了如图所示的改进.