题目内容
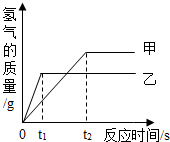 将等质量的甲、乙两金属分别与足量的稀硫酸反应,产生氢气的质量与反应时间的关系如图.关于甲、乙两金属判断合理的是( )
将等质量的甲、乙两金属分别与足量的稀硫酸反应,产生氢气的质量与反应时间的关系如图.关于甲、乙两金属判断合理的是( )| A、铁、锌 | B、锌、镁 |
| C、锌、铁 | D、铁、镁 |
考点:金属的化学性质
专题:金属与金属材料
分析:由题目的信息和图象可知:将等质量的甲、乙两金属分别与足量的稀硫酸反应,产生氢气的质量,甲比乙多,但是乙比甲活泼,因此甲、乙分别是铁和锌;不会是锌、镁,因为镁产生的氢气比锌又快又多;不会是锌、铁,正好颠倒了;不会是铁、镁,因为镁产生的氢气比铁又快又多.
解答:解:A、将等质量的甲、乙两金属分别与足量的稀硫酸反应,产生氢气的质量,甲比乙多,但是乙比甲活泼,因此甲、乙分别是铁和锌,故选项正确;
B、不会是锌、镁,因为镁产生的氢气比锌又快又多,故选项错误;
C、产生氢气的质量,甲比乙多,但是乙比甲活泼,因此甲、乙分别是铁和锌,不会是锌、铁,正好颠倒了,故选项错误;
D、不会是铁、镁,因为镁产生的氢气比铁又快又多,故选项错误;
故选A
B、不会是锌、镁,因为镁产生的氢气比锌又快又多,故选项错误;
C、产生氢气的质量,甲比乙多,但是乙比甲活泼,因此甲、乙分别是铁和锌,不会是锌、铁,正好颠倒了,故选项错误;
D、不会是铁、镁,因为镁产生的氢气比铁又快又多,故选项错误;
故选A
点评:本题考查了金属的性质,金属的活动性顺序是中考的重点内容之一,综合性比较强.经常出现在选择题、填空题和实验题中,同学们要认真掌握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
节能减排,保护环境,创造美丽泉城,是每个泉城人的义务.下列做法中,与此不相符的是( )
| A、选择自行车和公交车作为出行工具 |
| B、让衣服自然晾干,节约用纸,不使用一次性塑料袋 |
| C、将废纸、汽水瓶等收集起来,一次性焚烧 |
| D、拒绝一次性使用一次性木筷,用电子贺卡代替纸制贺卡 |
将甲、乙、丙三种金属分别放入稀硫酸中,只有甲产生气泡,将乙、丙放入硫酸铜溶液中,丙表面析出红色金属,乙没有明显现象.据此判断,三种金属的金属活动性顺序是( )
| A、甲>乙>丙 |
| B、乙>丙>甲 |
| C、丙>甲>乙 |
| D、甲>丙>乙 |
古语说:“人要实,火要虚”,其中“火要虚”的意思是说:燃烧木材时,通常要架空些,才能燃烧得更旺.“火要虚”的实质是( )
| A、散热的速度加快 |
| B、提高空气中氧气的含量 |
| C、降低木材的着火点 |
| D、增大木材与空气的接触面积 |
 在探究二氧化碳的性质时,证明二氧化碳能溶于水的实验,如图所示,试回答.
在探究二氧化碳的性质时,证明二氧化碳能溶于水的实验,如图所示,试回答.