题目内容
【题目】石英的主要成分为二氧化硅,它是玻璃工业和陶瓷工业的原料,冶金工业的助熔剂.
(1)二氧化硅的结构与金刚石相似,都是由__________(填“分子”、“原子”、或“离子”)构成的,二氧化硅属于__________(填“混合物”、“单质”或“氧化物”).
(2)装有氢氧化钠溶液的试剂瓶不能用玻璃塞,原因是在常温下,NaOH与玻璃塞中的SiO2缓慢地发生反应生成Na2SiO3和H2O.Na2SiO3使瓶口与瓶塞粘合在一起,则该反应的化学方程式为__________.
(3)硅是太阳能电池和电脑芯片不可缺少的材料.生产高纯硅的流程示意图如图:
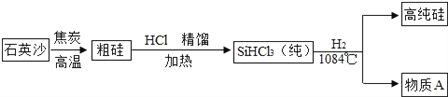
①制备粗硅的反应为:SiO2+2C![]() Si+2CO↑,反应的基本类型是__________(选“化合反应”或“分解反应”或“置换反应”)
Si+2CO↑,反应的基本类型是__________(选“化合反应”或“分解反应”或“置换反应”)
②整个制备过程必须达到无水无氧,若在H2还原SiHCl3过程中混入O2,可能引起的果是__________.
③为了达到绿色化学和节约资源的目的,物质A需要循环使用,A的化学式是__________.
【答案】 原子 氧化物 2NaOH+SiO2=Na2SiO3+H2O 置换反应 硅被氧化得不到高纯硅,且发生爆炸 HCl
【解析】本题在制取硅的情境下考查了物质的分类,反应类型,方程式的书写等,要仔细研读题目,结合已有的知识进行分析。
(1)金刚石是由碳原子构成的,二氧化硅的结构与金刚石相似,二氧化硅是由原子构成的,二氧化硅是由硅元素和氧元素组成的化合物,属于氧化物;
(2)NaOH与玻璃塞中的SiO2缓慢地发生反应生成Na2SiO3和H2O,其反应的化学方程式为2NaOH+SiO2=Na2SiO3+H2O;
(3)硅是太阳能电池和电脑芯片不可缺少的材料.由生产高纯硅的流程示意图可知:
①制备粗硅的反应为:SiO2+2C![]() Si+2CO↑,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物,反应的基本类型是置换反应;
Si+2CO↑,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物,反应的基本类型是置换反应;
②整个制备过程必须达到无水无氧,若在H2还原SiHCl3过程中混入O2,氢气不纯时,可能爆炸,硅被氧化得不到高纯硅;
③由生产高纯硅的流程示意图可知,为了达到绿色化学和节约资源的目的,物质A需要循环使用,A的化学式是HCl。

 高中必刷题系列答案
高中必刷题系列答案【题目】蔗糖是生活中常见的一种物质,某兴趣小组对“蔗糖的组成”进行了探究。
【作出猜想】小组同学认为绿色植物通过光合作用将二氧化碳和水转化成葡萄糖和氧气,葡萄糖进一步转化为蔗糖,故蔗糖中一定含有碳、氢元素,可能含有氧元素。
【实验探究】方案一:小明将蔗糖在氧气中燃烧,检验生成物中有水和二氧化碳,得出结论“蔗糖是由碳、氢、氧三种元素组成的”。你认为小明的方案______(填“合理”或“不合理”),理由是________________________________。
方案二:小刚用如图所示装置进行实验,实验开始先通入一会儿氮气,然后关闭弹簧夹,点燃酒精灯给蔗糖加强热。
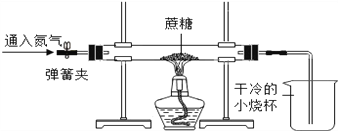
(1)观察到小烧杯中_______________,说明蔗糖中含有氢元素和氧元素。
(2)观察到硬质玻璃管中残留有黑色固体,他猜测该黑色固体是单质碳,并继续利用如图装置,另选试剂进行了验证单质碳的实验。实验过程和现象如表,请你将表格补充完整:
实验过程 | 实验现象 |
向小烧杯中加入适量__________(填试剂名称),往硬质玻璃管通入氧气,点燃酒精灯 | ①硬质玻璃管中的黑色固体剧烈燃烧,发出_______________,放热; ②烧杯中_____________________。 |
写出上述黑色固体燃烧的化学方程式_______________________________________。
【实验结论】蔗糖是由碳、氢、氧三种元素组成的。
【拓展交流】方案二中,先通入一会儿氮气的原因是___________________________。

