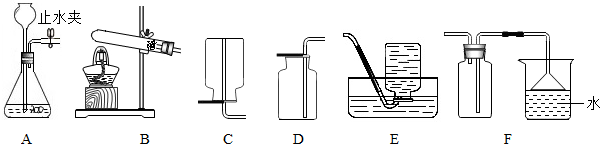
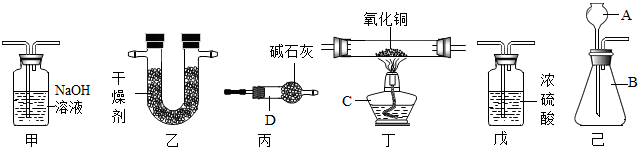
题目内容
某化学兴趣小组根据图1所示进行模拟炼铁的实验,并对产物成分及含量进行探究.
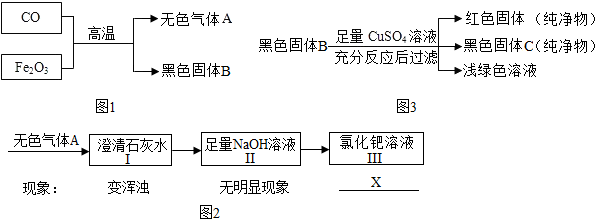
【提出问题】无色气体A有哪些成分?黑色固体B可能是什么?
【查阅资料】(1)常温下,一氧化碳能与氯化钯(PdCl2)溶液反应生成钯(不溶于水)、二氧化碳和氯化氢.
(2)铁的氧化物都能与稀盐酸、稀硫酸反应,其中氧化铁为红棕色,其余都为黑色,并且只有四氧化三铁能被磁铁吸引.
【提出猜想】猜想1:无色气体A一定是C02,原因是 (用化学方程式表示).
猜想2:黑色固体B全部是铁.
【交流与讨论】小华认为猜想1不一定正确,无色气体中除了CO2外,可能含有CO.
【探究反思】(1)为验证小华的猜想,大家按图2所示进行实验,过程与现象如下:
①当X现象为 时,可以确定猜想1是错误的,写出产生该现象的化学方程式: .
②Ⅱ中无明显现象,但可以往Ⅱ中滴加足量 (填试剂名称或化学式)证明气体在Ⅱ中确实已发生了反应.
(2)为验证猜想2,大家称取7g黑色固体B,按图3所示进行实验探究,过程与现象如下:
①经过分析,大家确定猜想2是错误的,理由是 .
②为了进一步确定黑色固体C的成分,你的方法是 (写出实验操作、现象及结论).
③实验结束后,称得红色固体的质量为6.4g,则黑色固体B中铁单质的质量分数为 .

【提出问题】无色气体A有哪些成分?黑色固体B可能是什么?
【查阅资料】(1)常温下,一氧化碳能与氯化钯(PdCl2)溶液反应生成钯(不溶于水)、二氧化碳和氯化氢.
(2)铁的氧化物都能与稀盐酸、稀硫酸反应,其中氧化铁为红棕色,其余都为黑色,并且只有四氧化三铁能被磁铁吸引.
【提出猜想】猜想1:无色气体A一定是C02,原因是
猜想2:黑色固体B全部是铁.
【交流与讨论】小华认为猜想1不一定正确,无色气体中除了CO2外,可能含有CO.
【探究反思】(1)为验证小华的猜想,大家按图2所示进行实验,过程与现象如下:
①当X现象为
②Ⅱ中无明显现象,但可以往Ⅱ中滴加足量
(2)为验证猜想2,大家称取7g黑色固体B,按图3所示进行实验探究,过程与现象如下:
①经过分析,大家确定猜想2是错误的,理由是
②为了进一步确定黑色固体C的成分,你的方法是
③实验结束后,称得红色固体的质量为6.4g,则黑色固体B中铁单质的质量分数为
考点:实验探究物质的组成成分以及含量,常见气体的检验与除杂方法,金属的化学性质,一氧化碳还原氧化铁,书写化学方程式、文字表达式、电离方程式,根据化学反应方程式的计算
专题:科学探究
分析:【提出猜想】
氧化铁和一氧化碳在高温条件下反应生成铁和二氧化碳;
【探究反思】
根据实验现象可以判断猜想是否正确;
根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式;
二氧化碳和氢氧化钠反应生成碳酸钠和水,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠;
铁和硫酸铜反应生成硫酸亚铁和铜;
根据实验现象可以判断物质的成分;
根据铜的质量可以计算铁的质量,进一步可以计算黑色固体B中铁单质的质量分数.
氧化铁和一氧化碳在高温条件下反应生成铁和二氧化碳;
【探究反思】
根据实验现象可以判断猜想是否正确;
根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式;
二氧化碳和氢氧化钠反应生成碳酸钠和水,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠;
铁和硫酸铜反应生成硫酸亚铁和铜;
根据实验现象可以判断物质的成分;
根据铜的质量可以计算铁的质量,进一步可以计算黑色固体B中铁单质的质量分数.
解答:解:【提出猜想】
猜想1:无色气体A一定是C02,原因是:氧化铁和一氧化碳反应生成二氧化碳,反应的化学方程式为:
Fe2O3+3CO
2Fe+3CO2.
故填:Fe2O3+3CO
2Fe+3CO2.
【探究反思】
(1)①当X现象为产生黑色沉淀时,可以确定猜想1是错误的,产生该现象的化学方程式为:
PdCl2+CO+H2O═Pd+CO2+2HCl.
故填:产生黑色沉淀;PdCl2+CO+H2O═Pd+CO2+2HCl.
②Ⅱ中无明显现象,但可以往Ⅱ中滴加足量CaCl2证明气体在Ⅱ中确实已发生了反应,因为氯化钙能和二氧化碳与氢氧化钠反应生成的碳酸钠反应生成白色沉淀--碳酸钙.
故填:CaCl2.
(2)①经过分析,大家确定猜想2是错误的,理由是:铁和足量硫酸铜反应生成硫酸亚铁和铜,不能产生黑色固体.
故填:铁和足量硫酸铜反应生成硫酸亚铁和铜,不能产生黑色固体.
②为了进一步确定黑色固体C的成分,实验方法是:实验操作:把磁铁靠近黑色固体;实验现象:黑色固体被吸引;实验结论:黑色固体是四氧化三铁.
实验操作:把适量黑色固体置于试管中,加入适量的稀硫酸;实验现象:溶液变成浅绿色;实验结论:黑色固体是氧化亚铁.
故填:实验操作:把磁铁靠近黑色固体;实验现象:黑色固体被吸引;实验结论:黑色固体是四氧化三铁.
实验操作:把适量黑色固体置于试管中,加入适量的稀硫酸;实验现象:溶液变成浅绿色;实验结论:黑色固体是氧化亚铁.
③设铁的质量为x,
Fe+CuSO4═FeSO4+Cu,
56 64
x 6.4g
=
,
x=5.6g,
则黑色固体B中铁单质的质量分数为:
×100%=80%.
故填:80%.
猜想1:无色气体A一定是C02,原因是:氧化铁和一氧化碳反应生成二氧化碳,反应的化学方程式为:
Fe2O3+3CO
| ||
故填:Fe2O3+3CO
| ||
【探究反思】
(1)①当X现象为产生黑色沉淀时,可以确定猜想1是错误的,产生该现象的化学方程式为:
PdCl2+CO+H2O═Pd+CO2+2HCl.
故填:产生黑色沉淀;PdCl2+CO+H2O═Pd+CO2+2HCl.
②Ⅱ中无明显现象,但可以往Ⅱ中滴加足量CaCl2证明气体在Ⅱ中确实已发生了反应,因为氯化钙能和二氧化碳与氢氧化钠反应生成的碳酸钠反应生成白色沉淀--碳酸钙.
故填:CaCl2.
(2)①经过分析,大家确定猜想2是错误的,理由是:铁和足量硫酸铜反应生成硫酸亚铁和铜,不能产生黑色固体.
故填:铁和足量硫酸铜反应生成硫酸亚铁和铜,不能产生黑色固体.
②为了进一步确定黑色固体C的成分,实验方法是:实验操作:把磁铁靠近黑色固体;实验现象:黑色固体被吸引;实验结论:黑色固体是四氧化三铁.
实验操作:把适量黑色固体置于试管中,加入适量的稀硫酸;实验现象:溶液变成浅绿色;实验结论:黑色固体是氧化亚铁.
故填:实验操作:把磁铁靠近黑色固体;实验现象:黑色固体被吸引;实验结论:黑色固体是四氧化三铁.
实验操作:把适量黑色固体置于试管中,加入适量的稀硫酸;实验现象:溶液变成浅绿色;实验结论:黑色固体是氧化亚铁.
③设铁的质量为x,
Fe+CuSO4═FeSO4+Cu,
56 64
x 6.4g
| 56 |
| x |
| 64 |
| 6.4g |
x=5.6g,
则黑色固体B中铁单质的质量分数为:
| 5.6g |
| 7g |
故填:80%.
点评:实验现象是物质之间相互作用的外在表现,正确的实验操作是得出科学结论的前提条件之一,因此要学会设计实验、进行实验、分析实验,为得出正确的结论奠定基础.

练习册系列答案
相关题目
醋酸、柠檬酸等是食品加工中常用的酸,之所以认为它们是酸,是因为( )
| A、它们都有酸味 |
| B、它们都能使紫色石蕊变红色 |
| C、它们电离产生的阳离子只有氢离子 |
| D、它们的PH小于7 |
下列物质鉴别的实验方法错误的是( )
| 鉴别物质 | 实验方法 |
| A.过氧化氢和蒸馏水 | 分别加入MnO2,看是否有气泡 |
| B.镁和锌 | 分别加入稀盐酸,看是否有气泡 |
| C、二氧化碳、氧气和空气 | 将燃着的木条分别伸入瓶中,观察现象 |
| D.活性炭和氧化铜 | 分别投入盛有红棕色二氧化氮气体的集气瓶中,观察现象 |
| A、过氧化氢和蒸馏水 |
| B、镁和锌 |
| C、二氧化碳、氧气和空气 |
| D、活性炭和氧化铜 |
下列所示的四个图象,与对应实验相符的( )
A、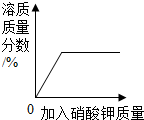 20℃时,向一杯饱和的KNO3溶液中加入KNO3晶体 |
B、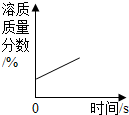 将一瓶浓硫酸敞口放置在空气中 |
C、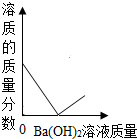 向装有稀硫酸的小烧杯中,不断滴加Ba(OH)2溶液至过量 |
D、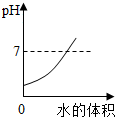 向pH=1的盐酸中不断加入水 |