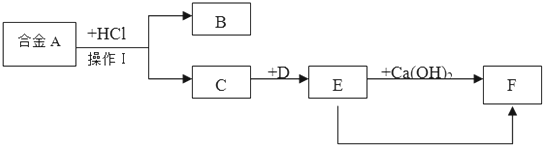
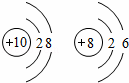题目内容
小娟想测定黄铜样品(铜锌合金)中铜的质量分数.她取该合金的粉末20g,与足量的稀硫酸充分反应后,经测定产生了0.2g气体.请你帮助她算出该合金中铜的质量分数.
| 根据化学反应方程式的计算.. | |
| 专题: | 有关化学方程式的计算. |
| 分析: | 根据生成氢气质量,由反应的化学方程式计算出产生合金中锌的质量,进而求出铜的质量以及该合金中铜的质量分数即可. |
| 解答: | 解:设参加反应的锌的质量为x. Zn+H2SO4=ZnSO4+H2↑ 65 2 x 0.2g
x=6.5g 合金中铜的质量分数为 答:合金中铜的质量分数为67.5%. |
| 点评: | 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,解题时要注意解题的规范性. |

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案
相关题目
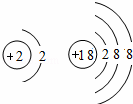
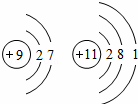
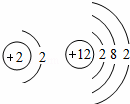
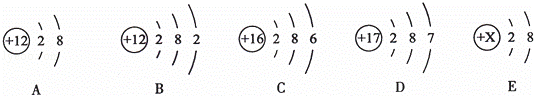
根据下列各组元素的原子结构示意图分析,具有相同化学性质的一组是( )
|
| A. |
| B. |
| C. |
| D. |
|
下列物质属于纯净物的是( )
|
| A. | 医用生理盐水 | B. | 碳酸饮料 | C. | 冰水混合物 | D. | 海水 |
下列图示中,试管的朝向与实验内容相符的是( )
|
| A. |
给液体加热 | B. |
开始装入固体药品 |
|
| C. |
排空气法收集氧气 | D. |
加热氯酸钾制氧 |
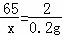
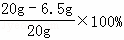 100%=67.5%
100%=67.5%