题目内容
海水是巨大的资源宝库.如图所示利用海水为原料可获得许多化工产品: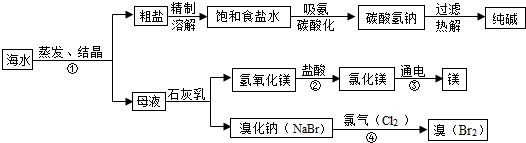
(1)步骤①中选用蒸发结晶法而不用降温结晶法的理由是 .
(2)制纯碱过程中,其中过滤操作所需要的玻璃仪器有烧杯、漏斗和 .
(3)步骤②发生反应的化学方程式是 ,其基本反应类型是 .用镁制造的一种镁铝合金常用作生产飞机外壳的材料,该材料具有的优良性能有 (任答一点).
(4)步骤④发生的反应为置换反应(类似于金属与盐溶液之间的反应),试写出该反应的化学方程式 .

(1)步骤①中选用蒸发结晶法而不用降温结晶法的理由是
(2)制纯碱过程中,其中过滤操作所需要的玻璃仪器有烧杯、漏斗和
(3)步骤②发生反应的化学方程式是
(4)步骤④发生的反应为置换反应(类似于金属与盐溶液之间的反应),试写出该反应的化学方程式
考点:对海洋资源的合理开发与利用,过滤的原理、方法及其应用,结晶的原理、方法及其应用,合金与合金的性质,酸的化学性质,书写化学方程式、文字表达式、电离方程式
专题:物质的制备
分析:根据氯化钠的溶解度受外界因素的影响进行分析;物质反应类型;正确书写化学方程式并注意规范性;正确理解和掌握合金的性能一般优于组成它的纯金属;了解物质的非金属性的强弱.
解答:解:
(1)步骤①中选用蒸发结晶法而不用降温结晶法的理由是:氯化钠的溶解度受温度影响很小.
故填:氯化钠的溶解度受温度影响很小.
(2)过滤操作所需要的仪器有烧杯、漏斗和玻璃棒.故填:玻璃棒.
(3)氢氧化镁和盐酸反应能生成氯化镁和水,反应的化学方程式为:Mg(OH)2+2HCl=MgCl2+2H2O.
该反应是两种化合物相互交换成分,生成另外两种化合物的反应,属于复分解反应.镁铝合金的优良性能有:强度高而密度又小,机械性能好,韧性和抗蚀性能很好.
故填:Mg(OH)2+2HCl=MgCl2+2H2O;复分解反应;强度高而密度又小,或机械性能好,或韧性和抗蚀性能很好.
(4)溴化钠和氯气反应能生成溴和氯化钠,反应的化学方程式为:2NaBr+Cl2═2NaCl+Br2.
故填:2NaBr+Cl2═2NaCl+Br2.
故答案为:
(1)氯化钠的溶解度受温度影响较小;(2)玻璃棒
(3)Mg(OH)2+2HCl=MgCl2+2H2O;复分解反应; 质量轻或强度大或抗腐蚀;
(4)2NaBr+Cl2=2NaCl+Br2
(1)步骤①中选用蒸发结晶法而不用降温结晶法的理由是:氯化钠的溶解度受温度影响很小.
故填:氯化钠的溶解度受温度影响很小.
(2)过滤操作所需要的仪器有烧杯、漏斗和玻璃棒.故填:玻璃棒.
(3)氢氧化镁和盐酸反应能生成氯化镁和水,反应的化学方程式为:Mg(OH)2+2HCl=MgCl2+2H2O.
该反应是两种化合物相互交换成分,生成另外两种化合物的反应,属于复分解反应.镁铝合金的优良性能有:强度高而密度又小,机械性能好,韧性和抗蚀性能很好.
故填:Mg(OH)2+2HCl=MgCl2+2H2O;复分解反应;强度高而密度又小,或机械性能好,或韧性和抗蚀性能很好.
(4)溴化钠和氯气反应能生成溴和氯化钠,反应的化学方程式为:2NaBr+Cl2═2NaCl+Br2.
故填:2NaBr+Cl2═2NaCl+Br2.
故答案为:
(1)氯化钠的溶解度受温度影响较小;(2)玻璃棒
(3)Mg(OH)2+2HCl=MgCl2+2H2O;复分解反应; 质量轻或强度大或抗腐蚀;
(4)2NaBr+Cl2=2NaCl+Br2
点评:本题考查了物质的溶解度受哪些因素影响,化学反应的类型,合金的性质,物质的非金属性大小,化学方程式的书写等多个知识点,是一个多点考查题.?

练习册系列答案
相关题目
 如图是某粒子的结构示意图,下列叙述正确的是( )
如图是某粒子的结构示意图,下列叙述正确的是( )| A、该粒子第一电子层有8个电子 |
| B、该粒子是阴离子 |
| C、该元素属稀有气体元素 |
| D、该粒子的核电荷数是18 |
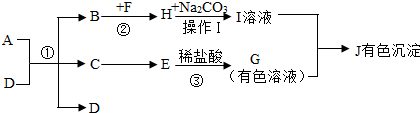
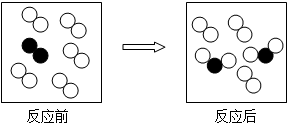 如图是某容器中的某个化学反应前、后物质变化的微观模拟图,请据图判断下列说法正确的是
如图是某容器中的某个化学反应前、后物质变化的微观模拟图,请据图判断下列说法正确的是 金属与我们的生活息息相关,在各个领域中用途广泛.
金属与我们的生活息息相关,在各个领域中用途广泛.


