题目内容
20.以下是某研究小组探究影响反应速率部分因素的相关实验数据.| 实验序号 | 过氧化氢溶液浓度/% | 过氧化氢溶液体积/ml | 温度/℃ | 二氧化锰的用量/g | 收集氧气的体积/ml | 反应所需的时间/S |
| ① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| ② | 12 | 1 | 20 | 0.1 | 4 | 6.04 |
| ③ | 30 | 5 | 35 | / | 2 | 49.21 |
| ④ | 30 | 5 | 55 | / | 2 | 10.76 |
(2)通过上述四个实验综合可知,影响化学反应速率的因素除催化剂外,还有反应物的浓度、温度等.
(3)用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总重量不变(选填“减小”或“不变”或“增大”).
分析 (1)根据图表中数据进行比较,找出不同点进行分析即可;
(2)利用控制变量法进行对比分析影响因素;
(3)根据生成物只与反应物量的多少有关,与反应物的浓度无关进行分析.
解答 解:(1)实验③和④对比可知反应所需的时间不同,反应所需的时间越短,说明反应得越快,再通过比较可知二者所用的温度不同,所以化学反应速率与温度有关,并且温度越高反应的越快;故填:在反应物浓度相同时,温度越高,化学反应速率越快;
(2)比较表格中的①②数据在其他条件都相同时,可以看出过氧化氢的浓度对反应速率的影响;比较表格中的④⑤数据在其他条件都相同时,可以看出反应温度度对反应速率的影响;故填:反应物的浓度、温度;
(3)加适量的水稀释后过氧化氢的浓度减小了,反应的速度慢了,但过氧化氢的质量并没有少,所以生成的氧气量不变;故填:不变.
点评 本题主要考查了能够影响化学反应的因素,解答这类题时要注意尽可能的把题中的能够影响化学反应的因素找出,然后再利用控制变量法来进行判断,最后得出答案.

练习册系列答案
相关题目
10.体操运动员在完成单杠、吊环项目时常用“镁粉”搓手,以起到防滑效果.某种“镁粉”中可能含有Mg、MgO、Mg(OH)2、MgCO3中的一种或两种固体,实验小组对其成分展开了探究.
已知:MgO+2HCl═MgCl2+H2O
MgCO3+2HCl═MgCl2+H2O+CO2↑
(1)探究“镁粉”中是否含有Mg和MgCO3
①取少量样品,如图1所示进行实验.观察到a试管中有气泡产生,b试管中产生的现象是澄清石灰水变浑浊.则证明“镁粉”中一定含有MgCO3.
②为证明“镁粉”中是否含有Mg,小明将燃着的木条放在图中b试管口上方,木条熄灭.但同学们指出,该实验不能达成实验目的,需要将图中的澄清石灰水替换成氢氧化钠浓溶液.小明按照修改后的实验方案重复上述实验,观察到b试管口无明显现象,证明“镁粉”中不含Mg.
(2)探究“镁粉”中是否还含有MgO及Mg(OH)2
【实验过程】
Ⅰ.用MgO、Mg(OH)2和MgCO3三种固体分别做性质实验.分别取0.5 g三种固体粉末,每次取样方法如图2所示:
逐滴加入相同溶质质量分数的稀盐酸直至粉末恰好消失.在下表中记录消耗的同浓度稀盐酸的体积(以下体积均在同一条件下测定,且保留到小数点后1位)
Mg(OH)2与盐酸发生中和反应的化学方程式为Mg(OH)2+2HCl═MgCl2+2H2O.
Ⅱ.取“镁粉”样品0.5g,加入上述稀盐酸至粉末恰好溶解.此时消耗稀盐酸的体积约为5.3mL.
【实验分析及结论】
“镁粉”不只含有MgCO3.理由是0.5gMgCO3消耗的盐酸体积与0.5g“镁粉”消耗的盐酸体积不相等
【实验反思】
为确定“镁粉”的具体成分,同学们认为还需要补充如下实验:分别取0.5g“镁粉”和0.5gMgCO3,加入足量稀盐酸,测定生成的气体体积分别为119mL和140mL.由此可知“镁粉”中含有MgCO3的质量分数为85%,“镁粉”中除MgCO3外的另一种物质为Mg(OH)2.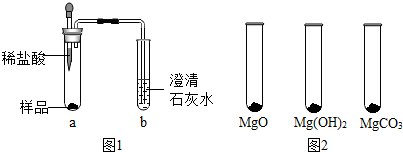
已知:MgO+2HCl═MgCl2+H2O
MgCO3+2HCl═MgCl2+H2O+CO2↑
(1)探究“镁粉”中是否含有Mg和MgCO3
①取少量样品,如图1所示进行实验.观察到a试管中有气泡产生,b试管中产生的现象是澄清石灰水变浑浊.则证明“镁粉”中一定含有MgCO3.
②为证明“镁粉”中是否含有Mg,小明将燃着的木条放在图中b试管口上方,木条熄灭.但同学们指出,该实验不能达成实验目的,需要将图中的澄清石灰水替换成氢氧化钠浓溶液.小明按照修改后的实验方案重复上述实验,观察到b试管口无明显现象,证明“镁粉”中不含Mg.
(2)探究“镁粉”中是否还含有MgO及Mg(OH)2
【实验过程】
Ⅰ.用MgO、Mg(OH)2和MgCO3三种固体分别做性质实验.分别取0.5 g三种固体粉末,每次取样方法如图2所示:
逐滴加入相同溶质质量分数的稀盐酸直至粉末恰好消失.在下表中记录消耗的同浓度稀盐酸的体积(以下体积均在同一条件下测定,且保留到小数点后1位)
| MgO | Mg(OH)2 | MgCO3 | |
| 消耗稀盐酸的体积/mL | 10.4 | 7.2 | 5.0 |
Ⅱ.取“镁粉”样品0.5g,加入上述稀盐酸至粉末恰好溶解.此时消耗稀盐酸的体积约为5.3mL.
【实验分析及结论】
“镁粉”不只含有MgCO3.理由是0.5gMgCO3消耗的盐酸体积与0.5g“镁粉”消耗的盐酸体积不相等
【实验反思】
为确定“镁粉”的具体成分,同学们认为还需要补充如下实验:分别取0.5g“镁粉”和0.5gMgCO3,加入足量稀盐酸,测定生成的气体体积分别为119mL和140mL.由此可知“镁粉”中含有MgCO3的质量分数为85%,“镁粉”中除MgCO3外的另一种物质为Mg(OH)2.

15. 如图是老师放置在实验桌上的三瓶无色气体,其中两瓶可能是O2和CO2.下列关于这三种气体的鉴别方法中,不正确的是( )
如图是老师放置在实验桌上的三瓶无色气体,其中两瓶可能是O2和CO2.下列关于这三种气体的鉴别方法中,不正确的是( )
 如图是老师放置在实验桌上的三瓶无色气体,其中两瓶可能是O2和CO2.下列关于这三种气体的鉴别方法中,不正确的是( )
如图是老师放置在实验桌上的三瓶无色气体,其中两瓶可能是O2和CO2.下列关于这三种气体的鉴别方法中,不正确的是( )| A. | 根据瓶③倒置,可判断瓶③存放的不可能是O2和CO2 | |
| B. | 用带火星的木条放入①中,若复燃,则存放的是O2 | |
| C. | 用点燃的木条伸入②中,若火焰熄灭,则存放的不是O2 | |
| D. | 向②中加入少量蒸馏水,若变为红色,则存放的是CO2 |
5.对下列实验指定容器中的水,其解释没有体现水的主要作用的是( )

①图Ⅰ烧杯中的水:形成密闭系统,观察检查时的现象
②图Ⅱ量筒中的水:通过水的体积变化得出O2的体积
③图Ⅲ集气瓶中的水:吸收放出的热量
④图Ⅳ集气瓶中的水:冷却溅落熔化物,防止集气瓶炸裂.

①图Ⅰ烧杯中的水:形成密闭系统,观察检查时的现象
②图Ⅱ量筒中的水:通过水的体积变化得出O2的体积
③图Ⅲ集气瓶中的水:吸收放出的热量
④图Ⅳ集气瓶中的水:冷却溅落熔化物,防止集气瓶炸裂.
| A. | ①②③④ | B. | ①②③ | C. | ①②④ | D. | ③ |
12.把众多原子划分为不同种元素的依据是( )
| A. | 原子质量 | B. | 原子半径 | C. | 核内中子数 | D. | 核内质子数 |
9.从化学方程式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5总结出的下列信息中,正确的是( )
①反应条件是点燃 ②反应前后元素的种类不变 ③反应前后分子的总数不变
④参加反应的物质是磷和氧气 ⑤P2O5是氧化物.
①反应条件是点燃 ②反应前后元素的种类不变 ③反应前后分子的总数不变
④参加反应的物质是磷和氧气 ⑤P2O5是氧化物.
| A. | ①②③⑤ | B. | ①②④⑤ | C. | ①③④ | D. | ②③④ |
10.维生素C(C6H8O6)主要存在于蔬菜和水果,它能促进人体生长发育.增强人体对疾病的抵抗力.近年来,科学家还发现维生素有防癌作用.下列关于维生素C的说法中错误的是( )
| A. | 青少年应多吃蔬菜水果,切忌偏食 | |
| B. | 维生素C中氧元素的质量分数约为54.5% | |
| C. | 维生素C中碳、氢、氧三种元素的质量比为9:1:12 | |
| D. | 维生素C由6个碳元素、8个氢元素、6个氧元素组成 |
 表示氧原子、
表示氧原子、 表示碳原子,
表示碳原子,