题目内容
11.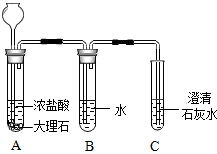 已知盐酸是HCI气体溶于水所形成的溶液,在实验室制取二氧化碳并检验其性质的实验中,如果用浓盐酸代替稀盐酸,并将产生的气体通入澄清的石灰水,往往看不到溶液变浑浊的现象,现有一同学用下列装置进行实验,却看到了澄清石灰水变浑浊的现象.
已知盐酸是HCI气体溶于水所形成的溶液,在实验室制取二氧化碳并检验其性质的实验中,如果用浓盐酸代替稀盐酸,并将产生的气体通入澄清的石灰水,往往看不到溶液变浑浊的现象,现有一同学用下列装置进行实验,却看到了澄清石灰水变浑浊的现象.回答下列问题:
(1)A 装置中发生反应的化学方程式是CaCO3+HCl=CaCl2+CO2↑+H2O;.
(2)B装置的作用是吸收氯化氢气体.此时B中的溶质为氯化氢.实验后向B中滴入石蕊溶液可看到的现象是变红;
(3)如果去掉B装置,将A与C直接相连,则C装置中可能发生反应的化学方程式为Ca(OH)2+2HCl=CaCl2+2H2O.(写一个即可)
分析 (1)根据盐酸和碳酸钙反应生成氯化钙、水和二氧化碳进行解答;
(2)根据浓盐酸具有挥发性以及氯化氢气体溶于水进行解答;
(3)根据浓盐酸具有挥发性,挥发出的氯化氢气体溶于水和澄清石灰水反应进行解答.
解答 解:(1)盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)浓盐酸具有挥发性以及氯化氢气体溶于水,所以B装置的作用是吸收挥发出的氯化氢气体;氯化氢气体溶于水显酸性,二氧化碳和水反应生成碳酸也呈酸性,所以实验后向B中滴入石蕊溶液,可看到的现象是石蕊溶液变红;
(3)浓盐酸具有挥发性,挥发出的氯化氢气体溶于水和澄清石灰水反应生成氯化钙和水,反应的化学方程式为Ca(OH)2+2HCl═CaCl2+2H2O.
故答案为:
(1)CaCO3+HCl=CaCl2+CO2↑+H2O;
(2)吸收氯化氢气体,氯化氢,变红;
(3)Ca(OH)2+2HCl=CaCl2+2H2O.
点评 了解实验数据处理或者误差分析的探究方法;掌握二氧化碳和酸的化学性质.

练习册系列答案
相关题目
1.在一个密闭容器中有X、Y、Z、Q四种物质,一定条件下充分反应,测得反应前后各物质的质量如表所示:
已知X和Q两种物质的相对分子质量均为M,下列推理中正确的是( )
| X | Y | Z | Q | |
| 反应前的质量/g | 8 | 10 | 1 | 21 |
| 反应后的质量/g | 0 | 21 | 待测 | 9 |
| A. | 反应后物质Z的质量为9g | |
| B. | 反应生成Y的质量为11g | |
| C. | 反应中物质Y与Q发生改变的质量之比为1:1 | |
| D. | 该反应的化学方程式中,物质X与Q的化学计量数之比为2:3 |
2.我省有许多历史悠久、闻名中外的传统工艺美术品.下列工艺品在制作过程中有新的物质生成的是( )
| A. |  黄山罗盘 | B. |  歙县歙砚 | C. |  徽州木雕 | D. |  界首彩陶 |
6.实验是学习化学的重要手段.下列实验设计不能达到实验目的是( )
| 选项 | 实验目的 | 实验设计[ |
| A | 确定NaOH溶液是否变质 | 滴加澄清石灰水观察现象 |
| B | 区别稀盐酸和稀硫酸 | 滴加氯化钡溶液观察现象 |
| C | 除去MnO2粉末中的KCl杂质 | 溶解、过滤、洗涤、干燥 |
| D | 检验Na2CO3溶液中是否含有NaCl杂质 | 滴加稀盐酸观察现象 |
| A. | A | B. | B | C. | C | D. | D |
16.3月20日,第三届重庆国际马拉松赛在南滨路落下帷幕,共有五万多名长跑爱好者参加了本次比赛,在下列参赛者所使用的物品中,属于天然纤维制品的是( )
| A. | 橡胶鞋底 | B. | 尼龙背包 | C. | 塑料水瓶 | D. | 纯棉毛巾 |