题目内容
下列有关实验操作、现象、解释或结论都正确的一组是( )
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 将水加入浓硫酸中配置成稀硫酸,将镁条置于其中 | 有气泡产生 | Mg是活泼金属 |
| B | 向溶液中加入过量的氯化钡溶液,过滤,在滤液中滴无色酚酞. | 产生白色沉淀,溶液呈红色 | 氢氧化钠部分变质 |
| C | 向一未知无色溶液中,加入适量的稀盐酸溶液 | 有无色气体产生 | 该无色未知溶液中一定有CO32- |
| D | 将ag的铁钉投入到硫酸铜溶液中,反应一段时间后,取出、洗净、烘干、称量为bg | 铁钉上覆盖一层红色的物质 | 金属活动顺序为:Fe>Cu,且析出铜的质量为(b-a)g |
| A、A | B、B | C、C | D、D |
考点:化学实验方案设计与评价,浓硫酸的性质及浓硫酸的稀释,金属的化学性质,酸的化学性质,碱的化学性质
专题:简单实验方案的设计与评价
分析:A、根据浓硫酸的稀释方法、酸的化学性质进行分析判断.
B、根据氯化钡能够和碳酸钠反应产生碳酸钡沉淀并除去碳酸钠排除对氢氧化钠碱性的干扰进行分析判断.
C、根据酸的化学性质进行分析判断.
D、根据金属的化学性质、质量守恒定律进行分析判断.
B、根据氯化钡能够和碳酸钠反应产生碳酸钡沉淀并除去碳酸钠排除对氢氧化钠碱性的干扰进行分析判断.
C、根据酸的化学性质进行分析判断.
D、根据金属的化学性质、质量守恒定律进行分析判断.
解答:解:A、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;一定不能把水注入浓硫酸中;故该实验操作错误.
B、氯化钡能够和碳酸钠反应产生碳酸钡沉淀并能除去碳酸钠排除对氢氧化钠碱性的干扰,再滴加酚酞试液变成红色,说明有氢氧化钠,说明氢氧化钠部分变质,故该实验操作、现象、解释或结论都正确.
C、碳酸盐、碳酸氢盐均能与盐酸反应都生成无色无味的气体,故可能含有碳酸根离子或碳酸氢根离子,故该无色未知溶液中也可能含有碳酸氢根离子,不一定有CO32-;故该实验结论错误.
D、将ag的铁钉投入到硫酸铜溶液中,铁钉上覆盖一层红色的物质,说明金属活动顺序为:Fe>Cu;反应一段时间后,取出、洗净、烘干、称量为bg,根据质量守恒定律可知,(b-a)g为固体质量增加的质量,而不是析出铜的质量,故选项结论错误.
故选:B.
B、氯化钡能够和碳酸钠反应产生碳酸钡沉淀并能除去碳酸钠排除对氢氧化钠碱性的干扰,再滴加酚酞试液变成红色,说明有氢氧化钠,说明氢氧化钠部分变质,故该实验操作、现象、解释或结论都正确.
C、碳酸盐、碳酸氢盐均能与盐酸反应都生成无色无味的气体,故可能含有碳酸根离子或碳酸氢根离子,故该无色未知溶液中也可能含有碳酸氢根离子,不一定有CO32-;故该实验结论错误.
D、将ag的铁钉投入到硫酸铜溶液中,铁钉上覆盖一层红色的物质,说明金属活动顺序为:Fe>Cu;反应一段时间后,取出、洗净、烘干、称量为bg,根据质量守恒定律可知,(b-a)g为固体质量增加的质量,而不是析出铜的质量,故选项结论错误.
故选:B.
点评:本题难度不是很大,掌握浓硫酸的稀释方法、酸、碱、盐的化学性质、金属的化学性质、质量守恒定律等是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
实验室有溶质质量分数为30%的氯化钾溶液,李晓取出一部分溶液,向其中加入60g水后溶质质量分数变为10%,则李晓稀释后的溶液中溶质质量为( )
| A、3g | B、9g |
| C、15g | D、18g |
实验室有一瓶无色气体,该气体可能是由H2、CH4、CO、CO2中的几种组成的.为了测定该瓶气体的成分,张乐进行了以下操作,根据实验现象判断下列说法正确的是( )
①将些混合气体通入盛有足量澄清的石灰水的烧杯中,杯中无明显现象;
②将气体干燥后点燃,罩在火焰上方的干燥烧杯内壁有水珠生成.
①将些混合气体通入盛有足量澄清的石灰水的烧杯中,杯中无明显现象;
②将气体干燥后点燃,罩在火焰上方的干燥烧杯内壁有水珠生成.
| A、A该混合气体中可能含有CO2 |
| B、该混合气体中一定含有H2 |
| C、该混合气体中一定含有CO |
| D、该混合气体可能是CH4和CO |
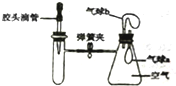 如图所示,装置气密性良好,弹簧夹处于关闭状态.挤压胶头滴管加入液体,一段时间后,打开弹簧夹,气球b不一定鼓起的是( )
如图所示,装置气密性良好,弹簧夹处于关闭状态.挤压胶头滴管加入液体,一段时间后,打开弹簧夹,气球b不一定鼓起的是( )| 试管内物质 | 胶头滴管内物质 | |
| A | 生石灰 | 水 |
| B | 镁条 | 稀盐酸 |
| C | 二氧化锰 | 过氧化氢 |
| D | 二氧化碳 | 氢氧化钠溶液 |
| A、A、 | B、B、 | C、C、 | D、D、 |
下列关于分子和原子的说法中,不正确的是( )
| A、分子、原子都在不停地运动 |
| B、分子是保持物质化学性质的最小粒子 |
| C、原子是不能再分的最小粒子 |
| D、在化学变化中,分子可以再分,而原子不可再分 |
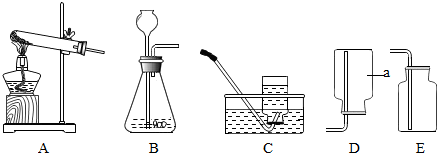
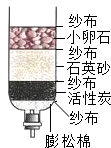 水是人类不可缺少的物质.
水是人类不可缺少的物质.