题目内容
12.小云同学对烧煮食物的某种固体酒精产生了浓厚的兴趣,于是她进行了以下探究活动.请你一起参与她的探究过程吧!【提出问题】:固体酒精是固态的酒精吗?
【查阅资料一】:酒精,学名乙醇,化学式为C2H6O,熔点为-114.1℃,沸点为78.5℃,易溶于水,能与水以任意比互溶.
【得出结论】:小云认为固体酒精不是固态的酒精,她作出该判断的理由是:酒精的熔点为-114.1℃,即在常温下,酒精不可能为固态.
【实验探究Ⅰ】:
取少量固体酒精置于蒸发皿中,用火柴点燃,固体酒精完全燃烧后,蒸发皿中残余了少量白色固体.
【提出新问题】:白色固体究竟是什么呢?
【查阅资料二】:由硬脂酸和氢氧化钠反应生成的硬脂酸钠作为凝固剂,酒精填充在硬脂酸钠骨架间隙中,即可得到固体酒精.固体酒精在较高的温度下燃烧时,硬脂酸钠可完全转化为硬脂酸和氢氧化钠,硬脂酸和酒精均可完全燃烧生成二氧化碳和水.
【实验探究Ⅱ】:请你完成以下实验报告.
| 序号 | 实验步骤 | 实验现象 | 实验结论 |
| ① | 用铂丝蘸取该固体在酒精灯上灼烧. | 火焰呈黄色 | 固体中含有Na+. |
| ② | 将该固体置于足量蒸馏水中. | 固体全部溶解. | 固体可溶于水. |
| ③ | 取少量②所得溶液,向其中滴加紫色石蕊试液,并振荡. | 溶液变蓝. | 溶液为碱性. |
| ④ | (此格不必填写) |
【联想与解释】小云联想到老师用玻璃导管将纯净的氢气导出并点燃时,燃烧火焰为黄色,其原因可能是:玻璃导管的成分中可能含有钠离子.
分析 【得出结论】:根据固体酒精若是固态的酒精的话,在常温下将是液态,因为酒精的熔点是-114.1℃进行解答;
【实验探究Ⅱ】:要证明氢氧化钠存在的方法是测定溶液显碱性,碳酸钠溶液也显碱性,所以要先证明碳酸钠的存在,并且把碳酸钠除去,再证明氢氧化钠的存在;
实验结论:根据碳酸钠和氯化钙反应生成碳酸钙沉淀,氢氧化钠溶液呈碱性进行解答;
【联想与解释】根据钠离子燃烧时火焰呈黄色进行解答.
解答 解:【得出结论】:酒精的熔点为-114.1℃,即在常温下,酒精不可能为固态,所以固体酒精不是固态的酒精;故填:酒精的熔点为-114.1℃,即在常温下,酒精不可能为固态;
[实验探究Ⅱ]:氢氧化钠溶液显碱性,通过测定溶液显碱性来确定氢氧化钠的存在.碳酸钠溶液也显碱性,会干扰氢氧化钠的检验,所以应先检验碳酸钠的存在,并将其除去,检验碳酸根离子用钙离子,但不能混入氢氧根离子,可用过量的氯化钙溶液,或硝酸钙溶液.故答案为
| 序号 | 实验步骤 | 实验现象 | 实验结论 |
| ④ | 取少量①所得溶液放入试管中,滴加过量氯化钙溶液,待充分反应后,滴加数滴无色酚酞试液. | 有白色沉淀生成, 溶液变红 | (此格不须填写) |
【联想与解释】:钠离子燃烧时火焰呈黄色,所以用玻璃导管将纯净的氢气导出并点燃时,燃烧火焰为黄色.故填:玻璃导管的成分中可能含有钠离子.
点评 检验混合物中的多种物质时,要注意检验的顺序,同时要把影响后面物质检验的物质除去.

练习册系列答案
相关题目
2.根据质量守恒定律,4g碳和4g氧气充分反应后,生成二氧化碳的质量是( )
| A. | 18 g | B. | 11 g | C. | 8 g | D. | 5.5 g |
3.写出下列溶液中的溶质和溶剂
| 溶液 | 碘酒 | 98%的浓硫酸 | 石灰水 | 生理盐水 | 酒精溶液 | 盐酸 | 硫酸铜溶液 |
| 溶质 | |||||||
| 溶剂 |
20.化学小组同学在课外读物中看到:“通常CO2可作灭火剂,但有些物质(如Na)着火,不能用CO2熄灭.”他们决定探究CO2与Na反应的产物.
【提出猜想】CO2与Na反应可能生成4种物质:C、CO、Na2O、Na2CO3.
【查阅资料】
①Na是非常活泼的金属,常温下与O2、H2O等物质反应.
②Na2O+H2O═2NaOH.
③向氯化钯(PdCl2)溶液中通入CO,产生黑色沉淀.
【实验过程】
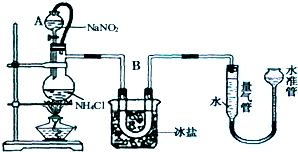
(1)设计实验:同学们在老师的指导下设计了如图所示装置(部分夹持仪器已略去)

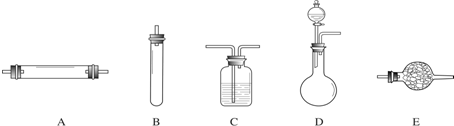
①盛放固体Na的仪器名称是硬质玻璃管;
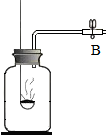
②为了得到纯净干燥的CO2气体,B、C中盛放的液体分别是NaHCO3溶液、浓硫酸,其中装置B的作用是净化吸收混有的氯化氢气体;
③装置尾端的气球作用是收集尾气,防止空气污染.
(2)实验记录
(3)实验反思
①实验记录②中,E中出现浑浊,再点燃酒精灯的目的是排出装置中的空气,防止空气的干扰.
②若无装置C,对实验有影响的物质是水.
③上述三个实验已经确认了三种物质的存在,验证另一物质是否存在的实验方案:
取D中白色固体于试管中,加水溶解,先加入过量的X试剂,过滤后,向滤液中再加入酚酞试液.
Ⅰ.X试剂可以选择下面何种物质D.
A.石灰水 B.Ca(OH)2溶液 C.稀盐酸 D.BaCl2溶液
Ⅱ.向滤液中再加入酚酞试液时,若出现溶液变红色现象时,说明第四种物质存在.
【提出猜想】CO2与Na反应可能生成4种物质:C、CO、Na2O、Na2CO3.
【查阅资料】
①Na是非常活泼的金属,常温下与O2、H2O等物质反应.
②Na2O+H2O═2NaOH.
③向氯化钯(PdCl2)溶液中通入CO,产生黑色沉淀.
【实验过程】
(1)设计实验:同学们在老师的指导下设计了如图所示装置(部分夹持仪器已略去)

①盛放固体Na的仪器名称是硬质玻璃管;
②为了得到纯净干燥的CO2气体,B、C中盛放的液体分别是NaHCO3溶液、浓硫酸,其中装置B的作用是净化吸收混有的氯化氢气体;
③装置尾端的气球作用是收集尾气,防止空气污染.
(2)实验记录
| 序号 | 实验操作 | 主要实验现象 | 实验结论和解释 |
| ① | 打开a,关闭b,由长颈漏斗注入稀盐酸 | A中产生大量气泡 E中出现浑浊 | E中反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O |
| ② | 当E中出现浑浊时,打开b,关闭a,点燃酒精灯 | D中Na剧烈燃烧,产生白烟内壁附着黑色、白色固体; G中产生黑色沉淀 | 反应产物一定有C和CO |
| ③ | 取D中白色固体于试管中,加水溶解,再加入石灰水 | 产生白色沉淀 | 反应产物还有Na2CO3;反应的方程式为Na2CO3+Ca(OH)2=CaCO3↓+2NaOH. |
①实验记录②中,E中出现浑浊,再点燃酒精灯的目的是排出装置中的空气,防止空气的干扰.
②若无装置C,对实验有影响的物质是水.
③上述三个实验已经确认了三种物质的存在,验证另一物质是否存在的实验方案:
取D中白色固体于试管中,加水溶解,先加入过量的X试剂,过滤后,向滤液中再加入酚酞试液.
Ⅰ.X试剂可以选择下面何种物质D.
A.石灰水 B.Ca(OH)2溶液 C.稀盐酸 D.BaCl2溶液
Ⅱ.向滤液中再加入酚酞试液时,若出现溶液变红色现象时,说明第四种物质存在.
17.下列关于氧气的说法中错误的是( )
| A. | 氧气约占空气总体积的$\frac{1}{5}$ | |
| B. | 氧气供给呼吸,它和体内物质反应,释放能量,维持生命活动的需要 | |
| C. | 氧气可以支持燃烧,说明氧气具有可燃性 | |
| D. | 夏天鱼池内需要增氧,是因为温度升高,氧气在水中的溶解度减小 |
 某同学在一次玩耍中,偶然发现竹子浸没水中后,在竹子上打一小洞,会看到水中有很多小气泡冒出.
某同学在一次玩耍中,偶然发现竹子浸没水中后,在竹子上打一小洞,会看到水中有很多小气泡冒出.