题目内容
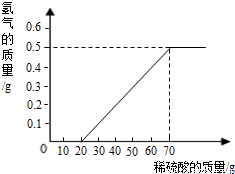
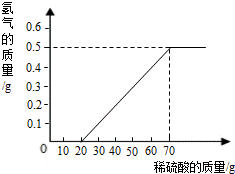
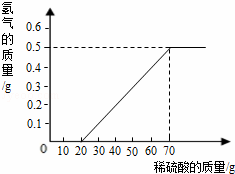
某兴趣小组用10g镁条与溶质质量分数为49%的稀硫酸反应.测得产生氢气的质量与稀硫酸的质量关系如图(假设镁条中除表面含有氧化镁外,没有其它杂质).
(1)当稀硫酸的质量为70g,产生的氢气的质量为 g.
(2)用化学方程式说明当稀硫酸的质量为10g时,为什么不产生氢气 .
(3)计算镁条中镁元素的质量分数(写出计算过程).
| (1)根据产生氢气的质量与稀硫酸的质量关系图,读出产生氢气的质量; (2)镁条的表面有氧化镁能与稀硫酸反应; (3)根据氧化镁、镁与稀硫酸反应的方程式以及镁之间的关系式求出镁的质量,再计算镁条中镁元素的质量分数. | |
| 解答: | 解:(1)由产生氢气的质量与稀硫酸的质量关系图可知,当稀硫酸的质量为70g,产生的氢气的质量为0.5g; (2)由于镁易于空气中的氧气反应在镁条的表面生成了氧化镁,稀硫酸首先与镁条表面的氧化镁薄膜发生了反应,所以不产生氢气,反应的方程式是:MgO+H2SO4=MgSO4+H2O. (3)设镁元素的质量为x 由Mg+H2SO4=MgSO4+H2↑ MgO+H2SO4=MgSO4+H2O 得:H2SO4~MgSO4~Mg 98 24 70g×49% x
镁条中镁元素的质量分数是: 故答为:(1)0.5(2)MgO+H2SO4=MgSO4+H2O;(3)84%. |

练习册系列答案
相关题目
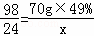 解得:x=8.4g
解得:x=8.4g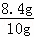 ×100%=84%
×100%=84%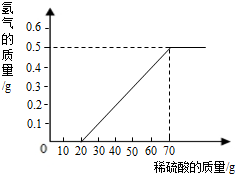 (2013?湛江)某兴趣小组用10g镁条与溶质质量分数为49%的稀硫酸反应.测得产生氢气的质量与稀硫酸的质量关系如图(假设镁条中除表面含有氧化镁外,没有其它杂质).
(2013?湛江)某兴趣小组用10g镁条与溶质质量分数为49%的稀硫酸反应.测得产生氢气的质量与稀硫酸的质量关系如图(假设镁条中除表面含有氧化镁外,没有其它杂质).