题目内容
11.用下面给定的五种粒子的结构示意图,完成下列问题(用符号或化学式填空,多个答案必须全部填写):
(1)属于原子的有H、Na、He;
(2)属于离子的有Na+、S2-;
(3)由原子构成的单质有Na、He;
(4)由离子构成的化合物有Na2S.
分析 (1)原子中核内质子数等于核外电子数;(2)原子中核内质子数不等于核外电子数,属于离子;(3)由原子构成的物质有:金属、非金属固体单质和稀有气体;(4)硫化钠属于离子化合物.
解答 解:(1)原子中核内质子数等于核外电子数,所以属于原子的是:H、Na、He;
(2)原子中核内质子数不等于核外电子数,属于离子,所以属于离子的是:Na+、S2-;
(3)由原子构成的物质有:金属、非金属固体单质和稀有气体,所以Na、He由原子构成;
(4)硫化钠属于离子化合物:Na2S.
故答案为:(1)H、Na、He;(2)Na+、S2-;(3)Na、He;(4)Na2S.
点评 解答本题关键是知道化学用语,熟悉化学式、元素符号的写法.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案
相关题目
1.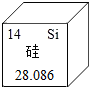 2013年度诺贝尔化学奖获得者的研究成 果是“发展多尺度模型研究复杂化学体系”,化学家们用计算机做“帮手”来揭示化学过程.晶体硅是制造计算机必不可少的材料,如图是硅元素的部分信息.下列有关说法正确的是( )
2013年度诺贝尔化学奖获得者的研究成 果是“发展多尺度模型研究复杂化学体系”,化学家们用计算机做“帮手”来揭示化学过程.晶体硅是制造计算机必不可少的材料,如图是硅元素的部分信息.下列有关说法正确的是( )
 2013年度诺贝尔化学奖获得者的研究成 果是“发展多尺度模型研究复杂化学体系”,化学家们用计算机做“帮手”来揭示化学过程.晶体硅是制造计算机必不可少的材料,如图是硅元素的部分信息.下列有关说法正确的是( )
2013年度诺贝尔化学奖获得者的研究成 果是“发展多尺度模型研究复杂化学体系”,化学家们用计算机做“帮手”来揭示化学过程.晶体硅是制造计算机必不可少的材料,如图是硅元素的部分信息.下列有关说法正确的是( )| A. | 相对原子质量为14 | B. | Si在地壳中含量最高 | ||
| C. | 单质硅不能用作导体 | D. | 原子核外有14个电子 |
3.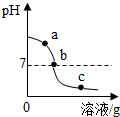 为探究氢氧化钙溶液和稀盐酸反应所得溶液中溶质的成分,小明和同学们通过测定了反应后溶液的pH,得到了如图所示的pH曲线,请回答:
为探究氢氧化钙溶液和稀盐酸反应所得溶液中溶质的成分,小明和同学们通过测定了反应后溶液的pH,得到了如图所示的pH曲线,请回答:
(1)由图可知该实验操作是将稀盐酸滴加到另一种溶液中;
(2)该反应的化学方程式为Ca(OH)2+2HCl═CaCl2+2H2O;
(3)实验过程中,小鸣取了a、b、c三处反应后的溶液于三个烧杯中,却忘了作标记,请你设计不同的方案(不再用测定pH的方法),探究三种样品分别属于哪处溶液.
【查阅资料】CaCl2溶液显中性,CaCl2+Na2CO3═CaCO3↓+2NaCl.
【探究过程】
①分别取少量样品于三支试管中,加入酚酞试液,观察到其中一支试管内出现溶液由无色变成红色的现象.结论:该样品是a处溶液.
②为进一步确定b或c处溶液,又设计了以下方案:
【反思评价】探究反应后溶液中溶质的成分,除了要考虑生成物之外,还要考虑反应物是否有剩余.
 为探究氢氧化钙溶液和稀盐酸反应所得溶液中溶质的成分,小明和同学们通过测定了反应后溶液的pH,得到了如图所示的pH曲线,请回答:
为探究氢氧化钙溶液和稀盐酸反应所得溶液中溶质的成分,小明和同学们通过测定了反应后溶液的pH,得到了如图所示的pH曲线,请回答:(1)由图可知该实验操作是将稀盐酸滴加到另一种溶液中;
(2)该反应的化学方程式为Ca(OH)2+2HCl═CaCl2+2H2O;
(3)实验过程中,小鸣取了a、b、c三处反应后的溶液于三个烧杯中,却忘了作标记,请你设计不同的方案(不再用测定pH的方法),探究三种样品分别属于哪处溶液.
【查阅资料】CaCl2溶液显中性,CaCl2+Na2CO3═CaCO3↓+2NaCl.
【探究过程】
①分别取少量样品于三支试管中,加入酚酞试液,观察到其中一支试管内出现溶液由无色变成红色的现象.结论:该样品是a处溶液.
②为进一步确定b或c处溶液,又设计了以下方案:
| 实验步骤 | 实验现象 | 实验结论 |
| 另取余下样品少量于两支试管中,分别滴加足量的Na2CO3溶液. | 只产生白色沉淀(产生白色沉淀也可) | 该样品为b处溶液. |
| 先产生气泡,后产生白色沉淀 | 该样品为c处溶液. |
1.如图所示操作正确的是( )
| A. | 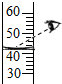 | B. |  | C. |  | D. |  |


