题目内容
14.相同质量的锌分别跟足量的稀盐酸、稀硫酸反应,产生的氢气的质量比为1:1.分析 根据Zn+2HCl=ZnCl2+H2↑,Zn+H2SO4=ZnSO4+H2↑,从反应可以看出,1个Zn原子置换一个H2分子,因此有多少锌就置换多少氢气,由于锌的质量相等,所以氢气的量也相等.
解答 解:反应的实质是锌和氢离子反应,足量的酸提供足量的氢离子,因此两个反应在本质上没有区别,故等质量的锌分别与足量的稀盐酸和稀硫酸反应后,产生氢气的质量是相等的.
故答案为:1:1
点评 本题考查了金属与酸反应生成氢气质量的计算,根据化学方程式、结合反应的实质,进行分析处理.

练习册系列答案
相关题目
4.物质X在水中反应的化学方程式为2X+2H2O→2Ca(OH)2+O2↑,其中X的化学式为( )
| A. | CaO | B. | CaO2 | C. | CaCO3 | D. | CaCl2 |
5.铜镁合金常用作飞机天线等导电材料,欲测定合金的组成(其他元素忽略不计),进行如下实验:取铜镁合金10g放入烧杯,将200g稀硫酸分4次加入烧杯中,充分反应后,测得剩余固体的质量记录如下.请计算
(1)铜镁合金中镁的质量.
(2)求所加稀硫酸中溶质的质量分数.(写出计算过程)
| 次 数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸质量/g | 50 | 50 | 50 | 50 |
| 剩余固体质量/g | 8.5 | 7 | 6.6 | 6.6 |
(2)求所加稀硫酸中溶质的质量分数.(写出计算过程)
9.下列实验现象描述不正确的是( )
| A. | 磷燃烧产生大量的白烟 | |
| B. | 硫在空气中燃烧产生淡蓝色火焰 | |
| C. | 电解水时正、负极产生气体体积比1:2 | |
| D. | 点燃棉线闻到烧焦羽毛气味 |
19.现有二瓶白色粉末:碳酸钡、硫酸钡.已知它们都不溶于水,请你想出鉴别方法(操作,步骤,结论):
| 分别取少量两种白色粉末于试管中,分别滴加稀盐酸 | 有气泡产生的是碳酸钡,无明显变化的是硫酸钡 |
1.我校科技探究小组收集到一批石灰石样品.为了测定该样品中碳酸钙的质量分数,同学们向不同质量的样品中加入100克稀盐酸,得到数据如下表.已知该样品中的杂质不溶于水,也不与盐酸反应.
请根据要求解答下列问题:
(1)将二氧化碳气体通入滴有紫色石蕊试液的蒸馏水中振荡,石蕊试液变红色.
(2)计算该石灰石样品中碳酸钙的质量分数.(精确到0.1%)
| 序号 | 1 | 2 | 3 |
| 稀盐酸的质量/g | 100 | 100 | 100 |
| 石灰石的质量/g | 8 | 18 | 28 |
| 二氧化碳的质量/g | 2.2 | 4.4 | 4.4 |
(1)将二氧化碳气体通入滴有紫色石蕊试液的蒸馏水中振荡,石蕊试液变红色.
(2)计算该石灰石样品中碳酸钙的质量分数.(精确到0.1%)
19.下列物质的用途是利用了其物理性质的是( )
| A. | 氧气急救病人 | B. | 氮气做保护气 | C. | 铜线做导线 | D. | 氢气做燃料 |
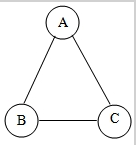 A、B、C是三种不同类别的含有氧元素的化合物,物质间相互反应的关系如图所示(图中“─”表示相连的两种物质能在溶液中发生反应).若B为纯碱,A、C间的反应为复分解反应,回答下列问题:
A、B、C是三种不同类别的含有氧元素的化合物,物质间相互反应的关系如图所示(图中“─”表示相连的两种物质能在溶液中发生反应).若B为纯碱,A、C间的反应为复分解反应,回答下列问题: