题目内容
14.元素周期表是学习和研究化学的重要工具,它的内容十分丰富.如表是依据元素周期表画出的1-18 号元素的原子结构示意图.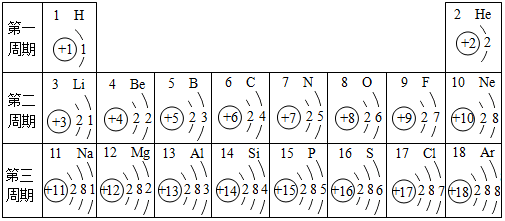
(1)上述表中是地壳含量最多的金属元素是铝元素,该元素的原子在化学反应中容易失(填“得”或“失”)电子,形成的离子符号为Al3+.
(2)从表中分析其规律可知,每一周期元素原子的电子层数相同.
(3)每一纵行我们称为同一族,从表中我们还可以分析得出,每族元素的原子的最外层电子数相同,由此我们猜想一下,第一纵行钠元素下面的钾元素的原子结构示意图为
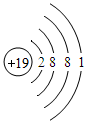 .
.
分析 (1)地壳含量最多的金属元素是铝元素,该元素的原子最外层电子数是3个,在化学反应中容易失电子,形成带3个单位正电荷的铝离子;
(2)电子层数相同的元素处在同一周期中;
(3)最外层电子数相同的元素存在同一族中;
钾原子的原子序数是19,据此可以书写钾原子的原子结构示意图.
解答 解:(1)上述表中是地壳含量最多的金属元素是铝元素,该元素的原子在化学反应中容易失电子,形成的离子符号为Al3+.
故填:铝元素;失;Al3+.
(2)从表中分析其规律可知,每一周期元素原子的电子层数相同.
故填:电子层数.
(3)每一纵行我们称为同一族,从表中我们还可以分析得出,每族元素的原子的最外层电子数相同,由此可知,第一纵行钠元素下面的钾元素的原子核内质子数是19,钾原子结构示意图为 .
.
故填:最外层电子数; .
.
点评 元素周期表反映了元素之间的内在联系,要注意理解和应用.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.工业铁红的主要成分是Fe2O3,还含有少量的FeO、Fe3O4.
为了测定铁红中铁的质量分数,兴趣小组的同学进行了如下实验,请你参与过程分析.
【资料1】草酸晶体(H2C2O4•3H2O)在浓H2SO4作用下受热分解,化学方程式为:
H2C2O4•3H2O$→_{△}^{浓H_{2}SO_{4}}$ CO2↑+CO↑+4H2O
(1)下列可用作草酸分解制取气体的装置是d(填字母编号).

【问题讨论】用图所示装置进行实验:
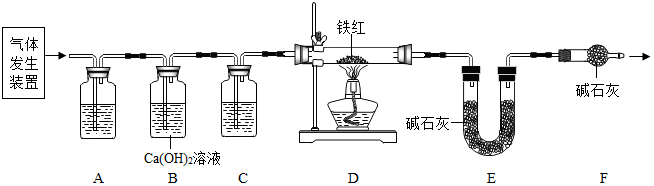
(2)实验前应先检查装置气密性.
(3)进入D中的气体是纯净、干燥的CO,则A、C中的试剂依次是c、a(填字母编号).
a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液
(4)B装置的作用是检验二氧化碳是否被氢氧化钠溶液完全吸收.
(5)对D装置加热前和停止加热后,都要通入过量的CO,其作用分别是:
①加热前排出装置中的空气,避免发生安全事故. ②停止加热后使反应生成的二氧化碳全部被碱石灰吸收.
(6)写出D装置中所发生反应的一个化学方程式Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,或FeO+CO$\frac{\underline{\;高温\;}}{\;}$Fe+CO2,或Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2.
【数据分析与计算】【资料2】铁的常见氧化物中铁的质量分数:
(7)称取铁红样品10.0g,用上述装置进行实验,测定铁红中铁的质量分数.
①D中充分反应后得到Fe粉的质量为m g,则14.0<m<15.56.
②实验前后称得E装置增重6.6g,则此铁红中铁的质量分数是76%.
【实验评价】
反思1:本实验中如果缺少C装置(不考虑其它因素),则测得样品中铁的质量分数会偏小(填“偏小”、“不变”或“偏大”).
反思2:请指出【问题讨论】中实验装置的一个明显缺陷没有处理尾气 .
为了测定铁红中铁的质量分数,兴趣小组的同学进行了如下实验,请你参与过程分析.
【资料1】草酸晶体(H2C2O4•3H2O)在浓H2SO4作用下受热分解,化学方程式为:
H2C2O4•3H2O$→_{△}^{浓H_{2}SO_{4}}$ CO2↑+CO↑+4H2O
(1)下列可用作草酸分解制取气体的装置是d(填字母编号).

【问题讨论】用图所示装置进行实验:

(2)实验前应先检查装置气密性.
(3)进入D中的气体是纯净、干燥的CO,则A、C中的试剂依次是c、a(填字母编号).
a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液
(4)B装置的作用是检验二氧化碳是否被氢氧化钠溶液完全吸收.
(5)对D装置加热前和停止加热后,都要通入过量的CO,其作用分别是:
①加热前排出装置中的空气,避免发生安全事故. ②停止加热后使反应生成的二氧化碳全部被碱石灰吸收.
(6)写出D装置中所发生反应的一个化学方程式Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,或FeO+CO$\frac{\underline{\;高温\;}}{\;}$Fe+CO2,或Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2.
【数据分析与计算】【资料2】铁的常见氧化物中铁的质量分数:
| 铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 铁的质量分数 | 77.8% | 70.0% | 72.4% |
①D中充分反应后得到Fe粉的质量为m g,则14.0<m<15.56.
②实验前后称得E装置增重6.6g,则此铁红中铁的质量分数是76%.
【实验评价】
反思1:本实验中如果缺少C装置(不考虑其它因素),则测得样品中铁的质量分数会偏小(填“偏小”、“不变”或“偏大”).
反思2:请指出【问题讨论】中实验装置的一个明显缺陷没有处理尾气 .
2.如图1是实验室制取气体的一些装置,据图回答有关问题.(友情提示:以下所选装置均填装置标号)
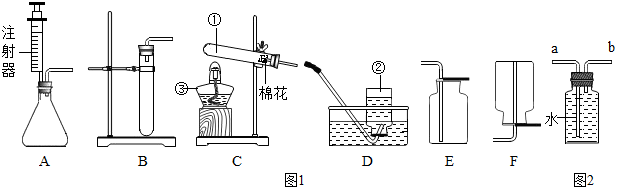
(1)写出序号为①②③的仪器名称:①试管;②集气瓶;③酒精灯.
(2)写出你知道的化学实验中可选用装置C制取气体的文字表式高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;
①该装置中试管口要略向下倾斜目的是防止水蒸气冷凝倒流炸裂试管
②收集所得气体可选用的一种装置是D
③如何检验收集的气体是氧气把带火星的木条伸到集气瓶中,木条复燃,证明是氧气.
(3)某学校化学兴趣小组在研究“带火星木条复燃与氧气体积分数的关系”的课题中,采取了以下实验步骤:①取5只250mL集气瓶,分别装入25mL、50mL、75mL、100mL、125mL的水,并用毛玻璃片盖住,依次编号为1、2、3、4、5;②用分解过氧化氢(H2O2)的方法制取氧气,用制取的氧气通过排水法将上述1~5号瓶中的水排去;③将带火星的木条依次插入1~5号瓶中,把观察到现象和计算数据,填入下表.
试回答下列问题:①实验室中采用分解过氧化氢(H2O2)的方法制取氧气,可采用的发生装置是(填标号)A或B,理由是反应物是固体和液体,反应条件不需加热其反应的文字表达式是过氧化氢$\stackrel{二氧化锰}{→}$水+氧气,该反应所属的基本反应类型是分解反应.
②根据以上实验事实,下列说法中正确的是B(填写相应的标号).
A.只有在纯氧中才能使带火星的木条复燃
B.集气瓶中氧气的体积分数≥52.6%时,带火星的木条就能复燃
C.只要有氧气存在就可使带火星的木条复燃
③上述实验表明:物质燃烧的程度与氧气的浓度有关,氧气浓度越大,燃烧越剧烈.请你再举一例,将实验内容和实验现象填写在下表中:
(4)实验室在常温下用块状电石与水反应制取微溶于水的乙炔气体,该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂.你认为上图中最适合制取乙炔气体的发生装置是A;如果用图2所示装置收集乙炔,气体应从b(填“a”或“b”)端管口通入.

(1)写出序号为①②③的仪器名称:①试管;②集气瓶;③酒精灯.
(2)写出你知道的化学实验中可选用装置C制取气体的文字表式高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;
①该装置中试管口要略向下倾斜目的是防止水蒸气冷凝倒流炸裂试管
②收集所得气体可选用的一种装置是D
③如何检验收集的气体是氧气把带火星的木条伸到集气瓶中,木条复燃,证明是氧气.
(3)某学校化学兴趣小组在研究“带火星木条复燃与氧气体积分数的关系”的课题中,采取了以下实验步骤:①取5只250mL集气瓶,分别装入25mL、50mL、75mL、100mL、125mL的水,并用毛玻璃片盖住,依次编号为1、2、3、4、5;②用分解过氧化氢(H2O2)的方法制取氧气,用制取的氧气通过排水法将上述1~5号瓶中的水排去;③将带火星的木条依次插入1~5号瓶中,把观察到现象和计算数据,填入下表.
| 集气瓶标号 | 1 | 2 | 3 | 4 | 5 |
| 集气瓶中氧气的体积分数 | 28.9% | 36.8% | 44.7% | 52.6% | 60.5% |
| 带火星木条的状况 | 微亮 | 亮 | 很亮 | 复燃 | 复燃 |
②根据以上实验事实,下列说法中正确的是B(填写相应的标号).
A.只有在纯氧中才能使带火星的木条复燃
B.集气瓶中氧气的体积分数≥52.6%时,带火星的木条就能复燃
C.只要有氧气存在就可使带火星的木条复燃
③上述实验表明:物质燃烧的程度与氧气的浓度有关,氧气浓度越大,燃烧越剧烈.请你再举一例,将实验内容和实验现象填写在下表中:
| 实验内容 | 实验现象 | 实验结论 |
| 氧气浓度越大,燃烧越剧烈 |
6.以下是四种微粒的结构示意图,有关各微粒的说法中,错误的是( )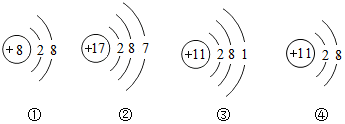

| A. | ①的化学性质比较稳定 | B. | ②容易得到电子 | ||
| C. | ③④属于同种元素 | D. | ④是一种阴离子 |

