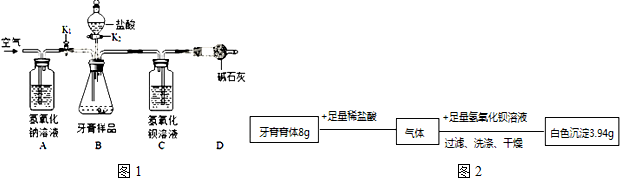
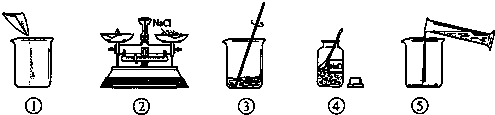
题目内容
18.实验室常用KClO3和MnO2质量比为5:1的固体混合物制取氧气.充分加热29.4g这种混合物.可生成多少克氧气?分析 氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,由题意,KClO3和MnO2质量比为5:1,充分加热29.4g这种混合物,据此计算出混合物中氯酸钾的质量,进而由反应的化学方程式计算出生成氧气的质量即可.
解答 解:29.4g这种混合物中氯酸钾的质量为29.4g×$\frac{5}{5+1}$=24.5g.
设可生成氧气的质量为x
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 96
24.5g x
$\frac{245}{96}=\frac{24.5g}{x}$ x=9.6g
答:可生成9.6g氧气.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
相关题目
5.下列产品的开发利用与保护环境无关的是( )
| A. | 无磷洗衣粉 | B. | 无氟冰箱 | C. | 加碘食盐 | D. | 无铅汽油 |
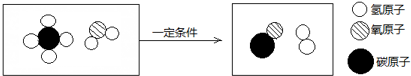
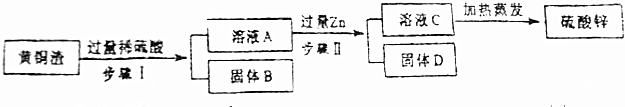 (1)步骤Ⅰ、Ⅱ中的操作为过滤.
(1)步骤Ⅰ、Ⅱ中的操作为过滤.