题目内容
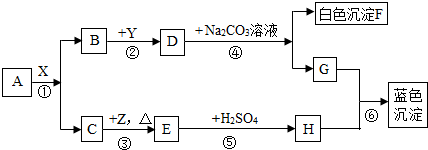
有四瓶失去标签的溶液:硝酸钡、碳酸钠、稀硫酸、盐酸.为了鉴别它们做了如下实验,根据现象推断A、B、C、D分别是什么物质,写出它们的化学式和有关的化学方程式.A和B混合有无色气体放出,D和B混合有无色气体放出 C和A混合没有明显现象.
则A是 B是 C是 D是 .
A+B的反应方程式 D+B的反应方程式 C+D的反应方程式 .
则A是
A+B的反应方程式
考点:酸、碱、盐的鉴别,书写化学方程式、文字表达式、电离方程式
专题:物质的鉴别题
分析:根据题意,四瓶失去标签的溶液:硝酸钡、碳酸钠、稀硫酸、盐酸,A和B混合有无色气体放出,D和B混合有无色气体放出,C和A混合没有明显现象,结合碳酸钠与稀硫酸、盐酸反应生成二氧化碳气体,则B为碳酸钠溶液;A和D为稀硫酸、稀盐酸,则C为硝酸钡;由于C和A混合没有明显现象,而硝酸钡与稀硫酸反应生成硫酸钡白色沉淀,与稀盐酸不反应,据此进行分析解答.
解答:解:四瓶失去标签的溶液:硝酸钡、碳酸钠、稀硫酸、盐酸,A和B混合有无色气体放出,D和B混合有无色气体放出,C和A混合没有明显现象,碳酸钠与稀硫酸、盐酸反应生成二氧化碳气体,则B为碳酸钠溶液;A和D为稀硫酸、稀盐酸,则C为硝酸钡;由于C和A混合没有明显现象,而硝酸钡与稀硫酸反应生成硫酸钡白色沉淀,与稀盐酸不反应,故A为稀盐酸,D为稀硫酸.
A+B反应生成氯化钠、水和二氧化碳,反应的化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑.
D+B反应生成硫酸钠、水和二氧化碳,反应的化学方程式为Na2CO3+H2SO4=Na2SO4+H2O+CO2↑.
C+D反应生成硫酸钡沉淀和硝酸,反应的化学方程式为H2SO4+Ba(NO3)2═BaSO4↓+2HNO3.
故答案为:HCl;Na2CO3;Ba(NO3)2;H2SO4;Na2CO3+2HCl═2NaCl+H2O+CO2↑;Na2CO3+H2SO4=Na2SO4+H2O+CO2↑;H2SO4+Ba(NO3)2═BaSO4↓+2HNO3.
A+B反应生成氯化钠、水和二氧化碳,反应的化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑.
D+B反应生成硫酸钠、水和二氧化碳,反应的化学方程式为Na2CO3+H2SO4=Na2SO4+H2O+CO2↑.
C+D反应生成硫酸钡沉淀和硝酸,反应的化学方程式为H2SO4+Ba(NO3)2═BaSO4↓+2HNO3.
故答案为:HCl;Na2CO3;Ba(NO3)2;H2SO4;Na2CO3+2HCl═2NaCl+H2O+CO2↑;Na2CO3+H2SO4=Na2SO4+H2O+CO2↑;H2SO4+Ba(NO3)2═BaSO4↓+2HNO3.
点评:本题有一定难度,解答不另加试剂就能鉴别的题目时,若都没有颜色,可将溶液两两混合,根据混合后的现象进行鉴别.

练习册系列答案
相关题目
由过氧化氢的化学式H2O2获得的下列认识中,错误的是( )
| A、属于氧化物 |
| B、由氢、氧两种元素组成 |
| C、与H2O的化学性质相同 |
| D、氢、氧元素质量比为1:16 |
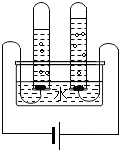 根据电解水的实验装置图完成下列问题:
根据电解水的实验装置图完成下列问题: