题目内容
9.实验小组进行了如下实验.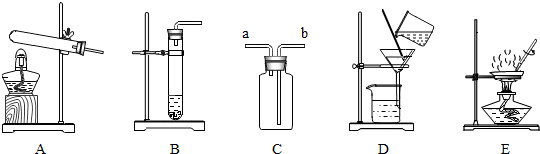
(1)实验室用装置A取氧气的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;.
(2)实验室用装置B可制取的气体是二氧化碳,氧气,氢气.
(3)用装置C收集二氧化碳,验满时,燃着木条应放在a(填“a”或“b”)端.
(4)实验室制取二氧化碳后,若从固液残留物中得到CaCl2固体,应进行的操作是过滤,蒸发.
分析 (1)根据实验室制氧气的原理及装置解答;
(2)根据实验室制二氧化碳的装置、原理进行解答;
(3)二氧化碳的密度比空气大;
(4)混合物分离的方法解答.
解答 解:(1)A装置是固体加热型装置,所以可用于高锰酸钾制氧气,方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)大理石是固体,稀盐酸是液体,反应条件是常温,过氧化氢制取氧气、实验室制取氢气均为固液常温反应,可选此装置;
(3)用装置C收集二氧化碳,因二氧化碳的密度比空气大,应长进短出,故验满时,燃着木条应放在a端;
(4)实验室制取二氧化碳后固液残留物中可溶的氯化钙和一些固溶性杂质,先过滤除去不溶性杂质,再蒸发结晶得到CaCl2固体.
故答案为:(1)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑; (2)CO2、O2 (3)a (4)过滤,蒸发.
点评 熟练掌握实验室制二氧化碳和氧气的原理、装置、收集方法是解答本题关健.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
19.人体结石有多种,其中一种含有较多的草酸钙(CaC2O4),CaC2O4中碳元素的化合价是( )
| A. | +3 | B. | +2 | C. | +1 | D. | +4 |
4.下列做法中,能减缓化学反应速率的是( )
| A. | 面团发酵时放在温热处 | B. | 人在进食时细细嚼食物 | ||
| C. | 将食品放入冰箱冷藏 | D. | 煤燃烧时向煤炉中鼓入空气 |
1.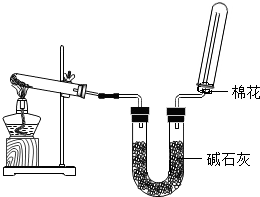 如图是制取氨气的装置图,原料为熟石灰和氯化铵固体.下列说法正确的是( )
如图是制取氨气的装置图,原料为熟石灰和氯化铵固体.下列说法正确的是( )
 如图是制取氨气的装置图,原料为熟石灰和氯化铵固体.下列说法正确的是( )
如图是制取氨气的装置图,原料为熟石灰和氯化铵固体.下列说法正确的是( )| A. | 直接给试管加热,不必进行预热 | |
| B. | 氨气的密度比空气大 | |
| C. | 将一湿润的蓝色石蕊试纸放在试管口,若变红,证明已满 | |
| D. | 铵态氮肥不能与碱性物质混合使用,以防氮肥损失 |
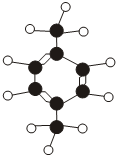 4月6日,福建古雷石化(PX项目)厂区发生爆炸,经过消防官兵几天的奋战,成功扑灭大火.PX是一种重要的化工原料,从化纤织物到食品包装,从医疗设备到家用电器,都要用到它的合成产物.PX的化学名称为对二甲苯,是一种低毒化合物,
4月6日,福建古雷石化(PX项目)厂区发生爆炸,经过消防官兵几天的奋战,成功扑灭大火.PX是一种重要的化工原料,从化纤织物到食品包装,从医疗设备到家用电器,都要用到它的合成产物.PX的化学名称为对二甲苯,是一种低毒化合物, ”代表碳原子.“
”代表碳原子.“ ”代表氢原子.试根据分子模型写出对二甲苯的化学式C8H10.
”代表氢原子.试根据分子模型写出对二甲苯的化学式C8H10. 生命吸管是能够将河水、泉水等直接过滤成直饮水的便携式净水装备.
生命吸管是能够将河水、泉水等直接过滤成直饮水的便携式净水装备.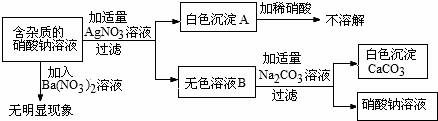
 ”和“
”和“ ”分别表示氧原子和汞原子.如图是氧化汞在加热条件下发生分解反应的微观模拟图.请回答下列问题:
”分别表示氧原子和汞原子.如图是氧化汞在加热条件下发生分解反应的微观模拟图.请回答下列问题: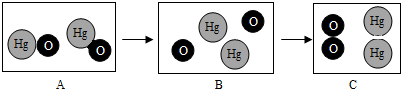
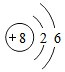 ;
;