题目内容
3.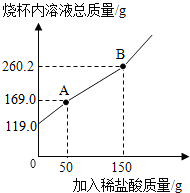 有一包含有碳酸钠和 碳酸氢钠的混合物,为了测定其含量,小明取19g样品放入烧杯中,加入100g水充分溶解后,逐渐滴入稀盐酸并不断搅拌,至B点时恰好完全反应.测出烧杯中溶液总质量与加入稀盐酸质量的关系曲线如图所示(反应生成的气体全部逸出).已知碳酸钠与稀盐酸反应分两步进行:
有一包含有碳酸钠和 碳酸氢钠的混合物,为了测定其含量,小明取19g样品放入烧杯中,加入100g水充分溶解后,逐渐滴入稀盐酸并不断搅拌,至B点时恰好完全反应.测出烧杯中溶液总质量与加入稀盐酸质量的关系曲线如图所示(反应生成的气体全部逸出).已知碳酸钠与稀盐酸反应分两步进行:第一步反应:Na2CO3+HCl═NaCl+NaHCO3
第二步反应:NaHCO3+HCl═NaCl+H2O+CO2↑
回答下列问题:
(1)A点溶液的溶质为NaHCO3、NaCl(填化学式)
(2)图中AB段表示第二步反应;根据质量守恒定律,反应后生成的二氧化碳质量是8.8g.
(3)所加入的稀盐酸中溶质质量分数是多少?(写出计算过程)(精确到0.1%)
(4)样品中碳酸氢钠的质量是8.4 g.
分析 (1)因为A点为第一步反应,则可推测A点溶液的溶质;
(2)图中AB段质量减少了,说明是第二步反应;
(3)根据第二步反应,加入的100g盐酸,由生成8.8g的二氧化碳气体可以得出盐酸的溶质质量,进一步可以计算加入的稀盐酸中溶质质量分数;
(4)由(2)盐酸的质量分数,求出50g中盐酸的质量,根据第一步反应即可求得Na2CO3质量,进一步可以计算样品中NaHCO3的质量.
解答 解:(1)因为A点为第一步反应Na2CO3+HCl═NaCl+NaHCO3,则可推测A点溶液的溶质为NaHCO3、NaCl;
(2)图中AB段质量减少了,表示第而二步反应;反应后生成的CO2质量为:19g+100g+150g-260.2g=8.8g.故填:二;8.8.
(3)设AB段稀盐酸中氯化氢的质量为x,
NaHCO3+HCl=NaCl+H2O+CO2↑,
36.5 44
x 8.8g
则$\frac{36.5}{44}=\frac{x}{8.8g}$,解得x=7.3g,
所加入的稀盐酸中溶质质量分数为:$\frac{7.3g}{150g-50g}$×100%=7.3%,
答:所加入的稀盐酸中溶质质量分数为7.3%.
(4)设碳酸钠的质量为y,
Na2CO3+HCl=NaCl+NaHCO3,
106 36.5
y 50g×7.3%
则$\frac{106}{36.5}=\frac{y}{50g×7.3%}$,解得y=10.6g,
答:样品中NaHCO3的质量为:19g-10.6g=8.4g.
故答案为:
(1)NaHCO3、NaCl; (2)二; 8.8; (3)7.3%;(4)8.4.
点评 差量法在计算中的应用很广泛,例如求二氧化碳的质量,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解.

| A. | 中和反应生成盐和水,则生成盐和水的反应一定是中和反应 | |
| B. | 化合物是由不同元素组成的纯净物,则由不同元素组成的纯净物一定是化合物 | |
| C. | 单质中只含有一种元素,则只含有一种元素的物质一定是单质 | |
| D. | 氧化物中含有氧元素,则含有氧元素的化合物一定是氧化物 |
| A. | 用熟石灰改良酸性土壤 | |
| B. | 用氢氧化钠溶液洗涤石油产品中的残留硫酸 | |
| C. | 用浓硫酸干燥湿润的氧气 | |
| D. | 服用含氢氧化铝的药物治疗胃酸过多 |
| A. | 生石灰干燥气体 | B. | 打开装浓盐酸的瓶盖冒白雾 | ||
| C. | 臭氧转化为氧气 | D. | 石墨变金刚石 |
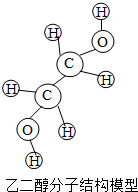 乙二醇是一种无色无臭、有甜味的液体,能与水以任意比例混合,可用作溶剂等.
乙二醇是一种无色无臭、有甜味的液体,能与水以任意比例混合,可用作溶剂等.下列有关乙二醇的叙述错误的是( )
| A. | 乙二醇的化学式为C2H602 | |
| B. | 乙二醇是由碳、氢、氧三种原子构成的 | |
| C. | 乙二醇与水不能形成饱和溶液 | |
| D. | 乙二醇可以用作汽车的防冻剂 |
| A. | 分离液态空气制取氧气是因为分子可以再分 | |
| B. | 水烧开后易把壶盖冲起是因为温度升高分子会变大 | |
| C. | 用洗洁精洗涤餐具上的油污是因为洗洁精是高效的溶剂 | |
| D. | 铝制品有抗腐蚀性能是因为表面生成了致密氧化膜起保护作用 |
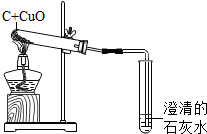 如图是碳和氧化铜在-定条件下进行反应的实验装置,该反应需几分钟时间.
如图是碳和氧化铜在-定条件下进行反应的实验装置,该反应需几分钟时间.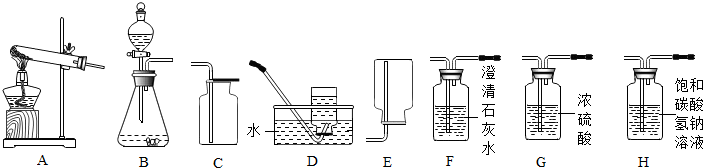
 氧气时一种化学性质比较活泼的气体,它能与许多物质发生化学反应.
氧气时一种化学性质比较活泼的气体,它能与许多物质发生化学反应.