题目内容
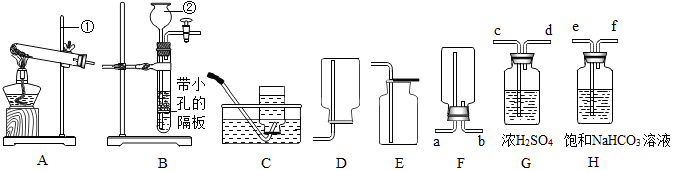
3.实验室部分装置如图所示,回答下列问题: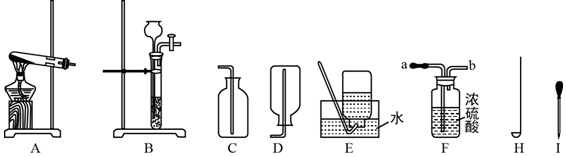
(1)写出图中标号仪器的名称:H燃烧匙,I胶头滴管.
(2)实验室用石灰石和稀盐酸反应制取并收集干燥的CO2,可选用的装置连接顺序为B→F→C,其反应原理是CaCO3+2HCl=CaCl2+CO2↑+H2O (用化学方程式表示).
(3)实验室常用A装置制氧气,该反应的化学方程式为2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑,若用E装置收集氧气,导致氧气不纯的主要原因是没有等到导管口处的气泡连续均匀冒出时就开始收集(或集气瓶实现没有灌满水),实验结束后,应先将导管从水中取出,再熄灭酒精灯,其目的是防止冷水倒吸,炸裂试管.
(4)实验室收集氨气不能用E装置,据此可知:氨气具有的性质是极易溶于水.
分析 (1)熟记仪器的名称;
(2)根据二氧化碳的制取、干燥与收集的顺序以及化学方程式的写法来分析;
(3)根据装置的特点、收集氧气的注意事项来分析;
(4)根据收集方法确定气体性质.
解答 解:(1)仪器H是燃烧匙;I是胶头滴管;故填:燃烧匙;胶头滴管;
(2)实验室中制取二氧化碳属于固液常温型,所以选择装置B来制取,制取的二氧化碳中混有水蒸气,应该用浓硫酸来进行干燥,最后用向上排空气法来收集;稀盐酸与大理石(或石灰石.其主要成分都是碳酸钙)反应生成氯化钙、水和二氧化碳,发生反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O;故填:B;F;C;CaCO3+2HCl=CaCl2+CO2↑+H2O;
(3)A装置适用于固体加热制取氧气,试管口没有棉花团,所以是在二氧化锰的催化作用下,加热氯酸钾制取氧气,同时生成氯化钾;若用排水法收集氧气,导致氧气不纯的主要原因可能是没有等到导管口处的气泡连续均匀冒出时就开始收集,或集气瓶实现没有灌满水;实验结束后,为了防止冷水倒吸,炸裂试管,应先将导管从水中取出,再熄灭酒精灯;故填:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑;没有等到导管口处的气泡连续均匀冒出时就开始收集(或集气瓶实现没有灌满水);防止冷水倒吸,炸裂试管;
(4)氨气极易溶于水,所以不能用排水法收集;故填:极易溶于水.
点评 本题难度不大,是中考的重要考点之一,熟练掌握实验室中制取气体的反应原理、发生装置和收集装置的选择依据等是正确解答本题的关键.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
20.甲、乙、丙、丁表示四种物质,其微观示意图见下表,甲和乙在一定条件下反应生成丙和丁.下列说法正确的是( )
 | 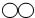 |  |  |  |
| 甲 | 乙 | 丙 | 丁 |
| A. | 甲、丁的化学式相同 | B. | 只有丙属于单质 | ||
| C. | 16g乙完全反应,可生成32g丙 | D. | 反应前后氧原子个数比为2:1 |
12.下列物质中属于纯净物的是( )
| A. | 空气中分离出来的稀有气体 | B. | 结冰的蒸馏水 | ||
| C. | 食盐水 | D. | 75%的医用酒精 |
13.你注意自己每天的食品中的营养搭配吗?下表是小明制定的食谱单,但明显存在搭配不当.
(1)为使营养均衡,在“你的补充”栏可以选填的食物是A.
A、凉拌黄瓜 B、糖醋鱼 C、熊掌豆腐 D、蛋糕
(2)主食中含有的主要营养物质是糖类(从六大营养物质中选取),当向馒头上滴加碘水后出现蓝色,说明馒头中含淀粉.
| 主食 | 米饭、馒头 |
| 副食 | 烧鸡块、咸鸭蛋、红烧鱼、花生米 |
| 饮料 | 牛奶 |
| 你的补充 |
A、凉拌黄瓜 B、糖醋鱼 C、熊掌豆腐 D、蛋糕
(2)主食中含有的主要营养物质是糖类(从六大营养物质中选取),当向馒头上滴加碘水后出现蓝色,说明馒头中含淀粉.
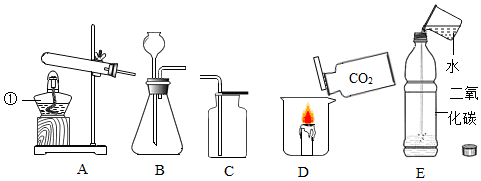
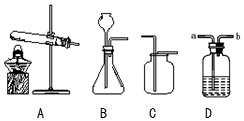 根据如图所示装置回答问题.
根据如图所示装置回答问题.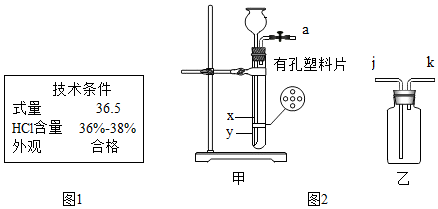 实验室制备二氧化碳的实验如下:
实验室制备二氧化碳的实验如下: