题目内容
2.结合图示实验装置,回答下列问题.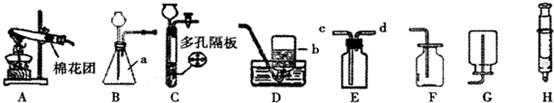
(1)写出装置中标号仪器的名称:a:锥形瓶b:集气瓶
(2)若用高锰酸钾制取氧气,应该选择的发生装置是A,发生的化学反应方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;若用F装置来收集O2验满的方法为将带火星的木条放在集气瓶瓶口,若木条复燃,则气体已经收集满.
(3)实验室制取CO2的化学方程式为CaCO3+2HCl═H2O+CaCl2+CO2↑,检验CO2的方法是:将产生的气体通入,观察到澄清石灰水浑浊,则是CO2.
(4)注射器H也可用于检查装置B的气密性,步骤如下:
①向锥形瓶中加入少量水没过长颈漏斗下端管口.②将注射器H连接到装置B的导管口处.③缓慢拉动注射器H的活塞,观察到长颈漏斗的下口有气泡冒出,表示装置B的气密性良好.
(5)实验室用装置C制取氢气,与装置B相比,其优点为可以控制反应的发生和停止;如用E装置收集H2,则气体应从端通入d(填“c”或“d”).
(6)用C装置在实验室制取CO2时,若多孔隔板改成隔离铜网,同样可以制取,如改用隔离铝丝网做,其产生的后果是二氧化碳中会混有杂质气体,用化学方程式表示为2Al+6HCl=2AlCl3+3H2↑,说明金属活动性Cu<Al(选填“>”、“<”或“=”).
分析 (1)熟记常见仪器的名称;
(2)根据高锰酸钾制取氧气的反应原理书写方程式;依据反应物和反应条件选择发生装置,根据氧气的助燃性来分析;
(3)根据实验室制取二氧化碳的反应原理书写方程式,并根据二氧化碳的性质进行检验;
(4)注射器H也可用于检查装置B的气密性:①向锥形瓶中加入少量水没过长颈漏斗下端管口.②将注射器H连接到装置B的导管口处.③缓慢拉动注射器H的活塞,观察到长颈漏斗的下口有气泡冒出,表示装置B的气密性良好;
(5)用装置C的优点是可以控制反应的发生和停止,根据氢气的密度来分析.
(6)根据铝和盐酸反应生成氯化铝和氢气,排在氢前面的金属可以置换出酸中的氢进行分析.
解答 解:(1)a是锥形瓶,b是集气瓶;故填:锥形瓶;集气瓶;
(2)高锰酸钾加热分解生成锰酸钾、二氧化锰和氧气;该反应属于加热固体的反应,所以选择发生装置A;将带火星的木条放在集气瓶瓶口,若木条复燃,则气体已经收集满;故填:A;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;将带火星的木条放在集气瓶瓶口,若木条复燃,则气体已经收集满;
(3)实验室制取二氧化碳用大理石与稀盐酸反应生成二氧化碳、氯化钙和水;检验二氧化碳用澄清石灰水,观察到澄清的石灰水变浑浊,是因为二者反应生成碳酸钙沉淀和水,反应的化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;故填:CaCO3+2HCl═H2O+CaCl2+CO2↑;澄清石灰水;澄清石灰水浑浊;
(4)注射器H也可用于检查装置B的气密性:①向锥形瓶中加入少量水没过长颈漏斗下端管口.②将注射器H连接到装置B的导管口处.③缓慢拉动注射器H的活塞,观察到长颈漏斗的下口有气泡冒出,表示装置B的气密性良好;故答案为:长颈漏斗的下口有气泡冒出;
(5)用装置C的优点是可以控制反应的发生和停止,氢气的密度比空气小,所以用装置E用来收集氢气时,气体从短管进入,故答案为:可以控制反应的发生和停止;d;
(6)铝和盐酸反应生成氯化铝和氢气,排在氢前面的金属可以置换出酸中的氢,所以化学方程式为:2Al+6HCl=2AlCl3+3H2↑,说明金属活动性Cu<Al.
故填:2Al+6HCl=2AlCl3+3H2↑;<.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

| A. | 烧杯、玻璃棒、漏斗、蒸发皿、酒精灯 | B. | 量筒、烧杯、试管夹、蒸发皿、铁架台 | ||
| C. | 漏斗、玻璃棒、镊子、蒸发皿、铁架台 | D. | 试管、量筒、药匙、玻璃棒、酒精灯 |
| A. | 花香袭人,是分子不断运动的反映 | |
| B. | 湿衣服放在火炉旁,干得较快,说明分子运动速率随温度升高而加快 | |
| C. | 温度升高,体温计中的水银体积变大,说明汞原子的体积发生了改变 | |
| D. | 氢气和液氢都可做燃料,说明同种物质的分子性质相同 |
| A. | 用酒精灯火焰直接加热烧杯 | |
| B. | 打开试剂瓶取用试剂后没及时盖瓶塞 | |
| C. | 将玻璃管一端润湿后,旋转着插入橡胶塞 | |
| D. | 取用试剂后将滴管清洗再放回原滴瓶 |
| A. | 石油的分馏 | B. | 白酒挥发 | C. | 饭菜变馊 | D. | 水结冰 |

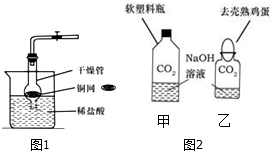
 某同学对一个储气筒内存放的气体探究如下:收集满两瓶气体,按如图所示进行实验,用带火星的木条分别以甲、乙两种方式迅速插入,发现木条复燃,木条在甲中燃烧比在乙中更旺.根据实验现象可得出结论是:该气体可能是氧气;
某同学对一个储气筒内存放的气体探究如下:收集满两瓶气体,按如图所示进行实验,用带火星的木条分别以甲、乙两种方式迅速插入,发现木条复燃,木条在甲中燃烧比在乙中更旺.根据实验现象可得出结论是:该气体可能是氧气;