题目内容
12.实验室用碳酸钙和盐酸反应来制取12.1克二氧化碳气体,问需与足量盐酸反应的碳酸钙多少克?分析 由二氧化碳的质量根据碳酸钙与盐酸反应的化学方程式可以计算出需要的碳酸钙的质量.
解答 解:设需要碳酸钙的质量为x.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 12.1g
$\frac{100}{x}$=$\frac{44}{12.1g}$
x=27.5g
答:需要碳酸钙的质量为27.5g.
点评 本题主要考查有关化学方程式的计算,难度较小.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
7.小明在做“酸碱中和反应”实验时,向盛有氢氧化钠溶液的烧杯中滴入几滴酚酞溶液,观察到溶液变红,接着,他又向其中加入一定量稀硫酸,发现红色褪去.
【提出问题】反应后所得溶液中溶质是什么?
【提出猜想】化学兴趣小组同学根据上述实验现象,一致认为反应后溶液中的溶质(除酚酞溶液外)一定有Na2SO4,理由是2NaOH+H2SO4=Na2SO4+2H2O(用化学方程式表示).
【设计方案】小红经过认真分析,认为反应后所得的溶液中还可能存在硫酸,并针对自己的猜想,设计了下列两种实验方案:
【反思评价】小组同学仔细研究上述两种实验方案后,认为方案1无法验证小红猜想的正确性,理由是硫酸钠和硫酸都能与硝酸钡溶液反应,生成白色沉淀,无法确定溶液中是否含有硫酸.
【拓展迁移】大家讨论后,按正确方案进行操作,确认了溶液中有硫酸存在,由此可知,在分析化学反应结束后所得物质的成分时,除了要考虑到生成物外,还有考虑到反应物是否有剩余.
【提出问题】反应后所得溶液中溶质是什么?
【提出猜想】化学兴趣小组同学根据上述实验现象,一致认为反应后溶液中的溶质(除酚酞溶液外)一定有Na2SO4,理由是2NaOH+H2SO4=Na2SO4+2H2O(用化学方程式表示).
【设计方案】小红经过认真分析,认为反应后所得的溶液中还可能存在硫酸,并针对自己的猜想,设计了下列两种实验方案:
| 实验方案 | 实验步骤 | 预期现象 | 结论 |
| 方案1 | 取样,滴入适量的硝酸钡溶液 | 出现白色沉淀 | 有硫酸 |
| 方案2 | 取样,滴入盛有锌粒的试管中 | 有气泡产生 | 有硫酸 |
【拓展迁移】大家讨论后,按正确方案进行操作,确认了溶液中有硫酸存在,由此可知,在分析化学反应结束后所得物质的成分时,除了要考虑到生成物外,还有考虑到反应物是否有剩余.
4.临近中考,小明将学过的化学知识整理如下.你认为完全正确的一组是( )
| A.除杂(括号内为杂质) | B.鉴别 |
| MnO2(KCl)-用水溶解、过滤、干燥 NaCl(Na2CO3)-加适量盐酸后蒸发 KNO3(NaCl)-降温结晶后过滤 | 磷肥和钾肥-观察颜色 羊毛和涤纶-点燃后嗅闻气味 硬水和软水-用肥皂水 |
| C.检验 | D.干燥 |
| 氧气-用带火星的木条检验 二氧化碳-用点燃的木条检验 盐酸-用pH试纸检验 | 氨气-用氢氧化钠固体干燥 二氧化碳-用生石灰干燥 氢气-用浓硫酸干燥 |
| A. | A | B. | B | C. | C | D. | D |
1.分析下列实验操作正确的是( )
| A. | 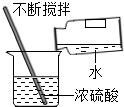 稀释浓硫酸 | B. |  称量氢氧化钠固体 | ||
| C. | 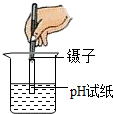 测定溶液的pH | D. | 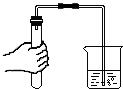 检查装置的气密性 |
2.某同学测定硫酸铜晶体(CuSO4•5H2O)里结晶水的含量,请回答下列问题:
(1)实验步骤为:①研磨 ②称量空坩埚和装有试样的坩埚的质量 ③加热 ④冷却 ⑤称量 ⑥重复③至⑤的操作,直到连续两次称量的质量差不超过0.1g为止 ⑦根据实验数据计算硫酸铜结晶水的含量.现有坩埚、坩埚钳、三脚架、泥三角、研钵、玻璃棒、干燥器、药匙、酒精灯、火柴、硫酸铜晶体样品等实验用品,进行该实验时,缺少的实验用品是托盘天平.实验步骤⑥的目的是使硫酸铜晶体中的结晶水完全失去.
(2)细心的同学发现在加热硫酸铜晶体时,会闻到刺激性气味,那分解的产物是什么呢?
查阅资料发现:硫酸铜受热分解生成氧化铜和气体,气体是由SO2、SO3、O2中的一种或几种;SO2、SO3都能被碱石灰(氢氧化钠和氧化钙混合物)吸收,SO2、SO3都能被氢氧化钠溶液吸收.同学利用如图装置探究硫酸铜受热分解生成的气体的成分(假设加热硫酸铜粉末直至完全分解).实验结果发现:用带火星的木条伸入集气瓶D,发现木条能复燃,说明气体中含有O2.已知硫酸铜粉末质量为10.0克,完全分解后,各装置的质量变化关系如下表所示:
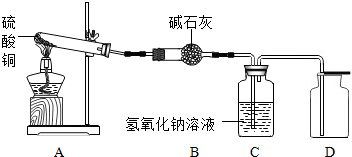
请通过计算,推断出该实验条件下硫酸铜分解的化学方程式是哪一个?B
A.3CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$3CuO+SO3↑+2SO2↑+O2↑ B.4CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$4CuO+2SO3↑+2SO2↑+O2↑
C.5CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$5CuO+SO3↑+4SO2↑+2O2↑ D.6CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$6CuO+4SO3↑+2SO2↑+O2↑
(1)实验步骤为:①研磨 ②称量空坩埚和装有试样的坩埚的质量 ③加热 ④冷却 ⑤称量 ⑥重复③至⑤的操作,直到连续两次称量的质量差不超过0.1g为止 ⑦根据实验数据计算硫酸铜结晶水的含量.现有坩埚、坩埚钳、三脚架、泥三角、研钵、玻璃棒、干燥器、药匙、酒精灯、火柴、硫酸铜晶体样品等实验用品,进行该实验时,缺少的实验用品是托盘天平.实验步骤⑥的目的是使硫酸铜晶体中的结晶水完全失去.
(2)细心的同学发现在加热硫酸铜晶体时,会闻到刺激性气味,那分解的产物是什么呢?
查阅资料发现:硫酸铜受热分解生成氧化铜和气体,气体是由SO2、SO3、O2中的一种或几种;SO2、SO3都能被碱石灰(氢氧化钠和氧化钙混合物)吸收,SO2、SO3都能被氢氧化钠溶液吸收.同学利用如图装置探究硫酸铜受热分解生成的气体的成分(假设加热硫酸铜粉末直至完全分解).实验结果发现:用带火星的木条伸入集气瓶D,发现木条能复燃,说明气体中含有O2.已知硫酸铜粉末质量为10.0克,完全分解后,各装置的质量变化关系如下表所示:

| 装置 | A(试管+粉末) | B | C |
| 反应前 | 42.0克 | 75.0克 | 140.0克 |
| 反应后 | 37.0克 | 79.5克 | 140.0克 |
A.3CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$3CuO+SO3↑+2SO2↑+O2↑ B.4CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$4CuO+2SO3↑+2SO2↑+O2↑
C.5CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$5CuO+SO3↑+4SO2↑+2O2↑ D.6CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$6CuO+4SO3↑+2SO2↑+O2↑
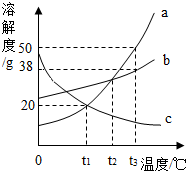 如图是a、b、c三种物质的溶解度曲线.根据图回答:
如图是a、b、c三种物质的溶解度曲线.根据图回答: