题目内容
15.(1)实验室要配制质量分数为6%的NaCl溶液100g.需要NaCl6g,水94g;(2)50g镁、锌、铁的混合物与足量的稀硫酸反应,将混合溶液蒸干后可得不含结晶水的固体146g,则反应生成氢气的质量为2g.
分析 (1)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;再根据溶剂质量=溶液质量-溶质质量即可求得水的质量.
(2)50g镁、锌、铁的混合物与足量的稀硫酸反应,反应后固体的质量增加是因M→MSO4(M是镁、锌、铁)是引起的,宜用差量法解答所需要的硫酸的质量,然后根据硫酸与氢气的对应关系求得所生成的氢气的质量.
解答 解:(1)溶质质量=溶液质量×溶质的质量分数,配制100g质量分数为6%的NaCl溶液,需氯化钠的质量=100g×6%=6g;溶剂质量=溶液质量-溶质质量,则所需水的质量=100g-6g=94g.
(2)以M代替三种金属,它们与硫酸反应的化学方程式可以表示为:
M+H2SO4=MSO4+H2↑
50g金属全部与SO42-结合,生成MSO4,质量增重146g-50g=96g.
设生成氢气为x
H2SO4~SO42-~H2
96 2
96g x
$\frac{96}{96g}=\frac{2}{x}$
x=2g,
所以生成氢气的质量为2g.
故答案为:(1)6;94;(2)2.
点评 本题难度不大,掌握溶质质量=溶液质量×溶质的质量分数、溶剂质量=溶液质量-溶质质量、利用反应物和生成物之间的质量差与反应中反应物、生成物的量成比例的关系进行计算的一种捷径是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.水是生命之源,有关水的认识正确的是( )
| A. | 生活中用活性炭降低水的硬度 | |
| B. | 液态水转化为水蒸气,水分子体积增大 | |
| C. | 水是相对分子质量最小的氧化物,在地球上储量丰富 | |
| D. | 从电解水得到H2和O2,可知水是由氢原子和氧原子组成的 |
3.下列实验仅利用家庭生活用品不可能完成的是( )
| A. | 用肥皂水鉴别自来水是软水还是硬水 | |
| B. | 探究蜡烛火焰各层温度的高低 | |
| C. | 用食腊除去热水瓶中的水垢 | |
| D. | 用加热法修补破裂的电木插座 |
20.X元素的原子最外层有6个电子,Y元素的原子最外层有三个电子,则由X和Y两种元素组成的化合物的化学式可能为( )
| A. | XY2 | B. | X2Y3 | C. | Y2X | D. | Y2X3 |
4.下列说法正确的是( )
| A. | 氯化钠溶液会加快钢铁的锈蚀 | |
| B. | 生铁能完全溶解在足量的稀硫酸中 | |
| C. | 高炉炼铁中所需的高温和CO的生成都与焦炭有关 | |
| D. | 多数合金的硬度低于组成它们的成分金属的硬度 |
2.下列实验操作正确的是( )
| A. |  给液体加热 | B. |  闻气体气味 | C. |  熄灭酒精灯 | D. |  读取液体体积 |
 元素周期表是学习化学的重要工具,如图是元素周期表中的一格,下面从该图获取的信息中,正确的是A
元素周期表是学习化学的重要工具,如图是元素周期表中的一格,下面从该图获取的信息中,正确的是A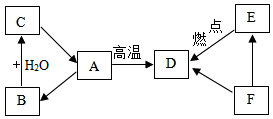 已知A、B、C三种物质含有同种金属元素,其中A是大理石的主要成分,B为氧化物;D、E、F 三种物质含有同种非金属元素,其中E与血红蛋白的结合力大约是氧气的200~300倍,F是单质.将A高温煅烧,得到B与D,它们之间的转化关系如图所示(有些转换关系,反应条件等略去),试回答:
已知A、B、C三种物质含有同种金属元素,其中A是大理石的主要成分,B为氧化物;D、E、F 三种物质含有同种非金属元素,其中E与血红蛋白的结合力大约是氧气的200~300倍,F是单质.将A高温煅烧,得到B与D,它们之间的转化关系如图所示(有些转换关系,反应条件等略去),试回答: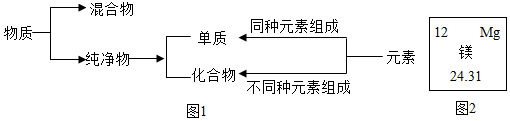
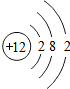 ,其氯化物的化学式为MgCl2.
,其氯化物的化学式为MgCl2.