题目内容
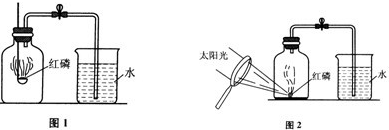
用来测定空气成分的方法很多,如图1所示是用红磷在空气中燃烧的测定方法.实验过程是:
第一步:将集气瓶容积划分为5等份,并做好标记.
第二步:点燃燃烧匙内的红磷,伸入集气瓶中并把塞子塞紧.
第三步:待红磷熄灭并冷却后,打开弹簧夹,发现水被吸入集气瓶中,进入集气瓶中水的体积约为集气瓶总容积的
.请回答下列问题:
(1)集气瓶中剩余的气体是 (填“纯净物”或“混合物”).
(2)实验完毕,若进入集气瓶中水的体积不到总容积的
,你认为导致这一结果的原因可能是
A、装置漏气 B、弹簧夹未夹紧 C、红磷过量
D、导管中有空气 E、红磷燃烧一结束就打开了弹簧夹
(3)某同学对实验进行反思后,提出了改进方法(如图2所示)你认为改进后的优点是: .
(4)小华用蜡烛代替红磷进行空气中O2含量测量,未达到实验目的,原因是 .
第一步:将集气瓶容积划分为5等份,并做好标记.
第二步:点燃燃烧匙内的红磷,伸入集气瓶中并把塞子塞紧.
第三步:待红磷熄灭并冷却后,打开弹簧夹,发现水被吸入集气瓶中,进入集气瓶中水的体积约为集气瓶总容积的
| 1 |
| 5 |

(1)集气瓶中剩余的气体是
(2)实验完毕,若进入集气瓶中水的体积不到总容积的
| 1 |
| 5 |
A、装置漏气 B、弹簧夹未夹紧 C、红磷过量
D、导管中有空气 E、红磷燃烧一结束就打开了弹簧夹
(3)某同学对实验进行反思后,提出了改进方法(如图2所示)你认为改进后的优点是:
(4)小华用蜡烛代替红磷进行空气中O2含量测量,未达到实验目的,原因是
考点:空气组成的测定,纯净物和混合物的判别
专题:空气与水
分析:(1)根据剩余空气的组成来分析;(2)利用红磷燃烧测定空气中氧气的含量时,如果操作不当,会导致测定的结果不准确.(3)不同的实验装置,功能不同;
(4)实验室测定空气中氧气的含量,药品选择在空气中只能与氧气反应,生成物是固体.
(4)实验室测定空气中氧气的含量,药品选择在空气中只能与氧气反应,生成物是固体.
解答:解:(1)集气瓶内剩余的气体有氮气、二氧化碳、稀有气体等,故为混合物;故填:混合物;
(2)如果装置漏气,红磷不足,没有冷却到室温就打开止水夹,都能够导致进入集气瓶中水的体积不到总容积的五分之一.
故填:AE.
(3)装置改进后,操作起来比较简单,同时防止了红磷燃烧的产物扩散到空气中污染环境.
故填:装置始终密闭,空气没有逸出,实验结果准确.
(4)蜡烛在空气中燃烧生成二氧化碳气体和水蒸气,二氧化碳气体占据了氧气的空间,不能测定空气中氧气的含量.
故填:生成的二氧化碳是气体,瓶内气压未减小.
(2)如果装置漏气,红磷不足,没有冷却到室温就打开止水夹,都能够导致进入集气瓶中水的体积不到总容积的五分之一.
故填:AE.
(3)装置改进后,操作起来比较简单,同时防止了红磷燃烧的产物扩散到空气中污染环境.
故填:装置始终密闭,空气没有逸出,实验结果准确.
(4)蜡烛在空气中燃烧生成二氧化碳气体和水蒸气,二氧化碳气体占据了氧气的空间,不能测定空气中氧气的含量.
故填:生成的二氧化碳是气体,瓶内气压未减小.
点评:可以用来测定空气中氧气含量的物质应该具备的条件是:能和空气中的氧气反应,生成物是固体,不能和空气中的其它物质发生化学反应.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
通过如图所示实验得出的结论中,正确的是( )
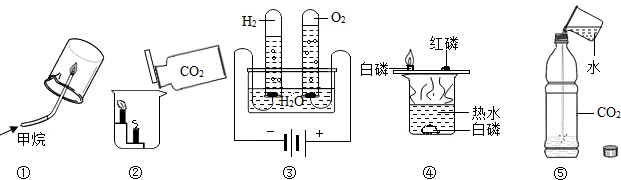
①既可说明甲烷具有可燃性,又说明了甲烷是由氢元素和碳元素组成
②既可说明二氧化碳的密度比空气大,又说明了二氧化碳不能燃烧也不支持燃烧
③既可说明水分解能产生氢气和氧气,又说明了水是由氢元素和氧元素组成
④既可探究可燃物的燃烧条件,又说明了白磷的着火点比红磷低
⑤既可说明二氧化碳能溶于水,又说明了二氧化碳具有酸性.

①既可说明甲烷具有可燃性,又说明了甲烷是由氢元素和碳元素组成
②既可说明二氧化碳的密度比空气大,又说明了二氧化碳不能燃烧也不支持燃烧
③既可说明水分解能产生氢气和氧气,又说明了水是由氢元素和氧元素组成
④既可探究可燃物的燃烧条件,又说明了白磷的着火点比红磷低
⑤既可说明二氧化碳能溶于水,又说明了二氧化碳具有酸性.
| A、②③④ | B、②③④⑤ |
| C、①②③④⑤ | D、①②③④ |
下列对实验基本操作的说法,有明显错误的是( )
| A、加热较多量液体时,可以用烧杯做容器 |
| B、滴瓶上的滴管可以通用滴加液体 |
| C、排水集气时应先向集气瓶内注满水 |
| D、加热试管应擦干试管外壁上的水珠 |
下列关于二氧化碳的说法正确的是( )
| A、实验室制取二氧化碳气体,装药品时先倒入稀盐酸后加入石灰石 |
| B、可用燃烧的木条检验一瓶无色、无味的气体是否是二氧化碳 |
| C、充满二氧化碳的集气瓶,盖好玻璃片后应倒放在桌面上以免泄露 |
| D、在实验室用大理石跟浓盐酸反应制取二氧化碳,将此二氧化碳通入澄清石灰水中,可能看不倒变浑 |
下列实验操作,错误的是( )
A、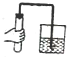 检查装置的气密性 |
B、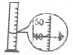 读取水的体积 |
C、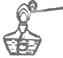 点燃酒精灯 |
D、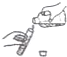 倾倒液体 |
下列图示的实验基本操作正确的是( )
A、 向试管中滴 |
B、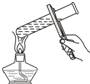 给试管中体液加热 |
C、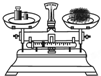 称量一定质量的食盐 |
D、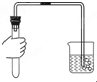 检查装置的气密性 |
为鉴别空气、氧气、二氧化碳三瓶气体,可选用的方法是( )
| A、将水倒入三瓶气体中 |
| B、将澄清的石灰水倒入三瓶气体中 |
| C、闻三瓶气体的气味 |
| D、将燃着的木条分别伸入三瓶气体中 |