题目内容
12.在日常生活中有一种杀菌、消毒剂主要就是过氧乙酸消毒溶液,具体的使用方法有浸泡法、擦拭法、喷雾法和熏蒸法,分别适用于小件物品、大件物品、室内空气及周围环境,过氧乙酸的化学式是:C2H4O3.根据过氧乙酸的化学式回答下列问题:(1)它是由3种元素组成;一个过氧乙酸分子中共有9个原子;
(2)过氧乙酸中,C、H、O三种元素的质量比是:6:1:12;
(3)过氧乙酸分子中C、H、O的原子个数比为2:4:3;
(4)过氧乙酸的相对分子质量是:76;其中氧元素的质量分数是:63.2%;
(5)152克过氧乙酸中含氧元素的质量是:96g.
分析 (1)根据过氧乙酸的化学式为CH3COOOH,来分析其元素组成;
(2)化合物中各元素质量比=各原子的相对原子质量×原子个数之比;
(3)根据分子结构来分析;
(4)根据相对分子质量和元素质量分数的计算方法分析;
(5)根据元素的质量=化合物的质量×化合物中元素的质量分数.
解答 解:(1)由过氧乙酸的化学式为CH3COOOH,则该物质是由碳、氢、氧三种元素组成,共有2个碳原子、3个氧原子、4个氢原子组成;故填:3;9;
(2)过氧乙酸中碳、氢、氧三种元素的质量比为C:H:O=(12×2):(1×4):(16×3)=6:1:12;故填:6:1:12;
(3)由过氧乙酸的化学式为CH3COOOH,1个过氧乙酸分子中含有2个碳原子、3个氧原子、4个氢原子组成,过氧乙酸分子中C、H、O的原子个数比为2:4:3;故填:2:4:3;
(4)过氧乙酸的相对分子质量为12×2+1×4+16×3=76,其中氧元素的质量分数是$\frac{16×3}{76}×100%$≈63.2%;故填:76;63.2%;
(5)152g过氧乙酸中含氧元素的质量是152g×$\frac{16×3}{76}×100%$=96g;故填:96g.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.红枣包装中常使用一种“504双吸剂”,其成分为铁粉、生石灰等.实验小组同学对一包使用过的“504双吸剂”进行了如下探究.
【提出问题】久置后,固体的成分是什么?
【查阅资料】(1)铁与氯化铁溶液在常温下发生反应生成氯化亚铁;
(2)铁可以被磁铁吸引,Fe2O3、CaO、Ca(OH)2、CaCO3均不被磁铁吸引.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【实验探究】实验方案一:
【实验分析】
(1)酚酞溶液颜色发生改变是因为溶液中含有OH-(填离子符号)离子;甲同学认为通过实验不能得出一定含Ca(OH)2的结论,理由是CaO+H2O=Ca(OH)2(用化学方程式表示),该反应的基本类型为化合反应.
(2)乙同学认为通过实验不能得出一定不含Fe2O3的结论,理由是氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色.她设计实验方案二继续进行探究.
实验方案二:
【实验分析】
(1)④中发生的两个复分解反应的化学方程式是Na2CO3+2HCl=2NaCl+H2O+CO2↑、Fe2O3+6HCl=2FeCl3+3H2O.
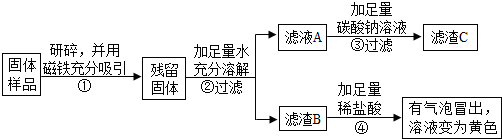
(2)通过实验二可确定固体样品中一定还含有Fe2O3.
(3)为确定固体样品中是否含有氢氧化钙,实验小组同学又经过实验测得上述残留固体总质量为1.66g,滤渣B质量为1.0g,滤渣C的质量为1.0g.
【实验结论】综合上述实验及所给数据,可判断实验小组同学们的猜想成立(填“成立”或“不成立”).
【实验反思】探究硫酸和氢氧化钠反应后硫酸是否有剩余,还可选择一种试剂紫色石蕊试液.
【提出问题】久置后,固体的成分是什么?
【查阅资料】(1)铁与氯化铁溶液在常温下发生反应生成氯化亚铁;
(2)铁可以被磁铁吸引,Fe2O3、CaO、Ca(OH)2、CaCO3均不被磁铁吸引.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【实验探究】实验方案一:
| 实验操作 | 实验现象 | 实验结论 |
| (1)取适量固体放于烧杯中,加足量蒸馏水溶解,静置后取上层清液,滴加无色酚酞溶液 | 固体溶解时烧杯外壁发烫 | 固体中一定含有①氧化钙 |
| 酚酞溶液变为②红色 | 固体中一定含有氢氧化钙 | |
| (2)另取少量固体放于试管中,滴加足量的盐酸 | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液 | 固体中一定含有③铁,一定不含Fe2O3 |
| (3)将步骤(2)中产生的气体通入到澄清的石灰水中 | 澄清石灰水变浑浊 | 固体中一定含有④CaCO3 |
(1)酚酞溶液颜色发生改变是因为溶液中含有OH-(填离子符号)离子;甲同学认为通过实验不能得出一定含Ca(OH)2的结论,理由是CaO+H2O=Ca(OH)2(用化学方程式表示),该反应的基本类型为化合反应.
(2)乙同学认为通过实验不能得出一定不含Fe2O3的结论,理由是氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色.她设计实验方案二继续进行探究.
实验方案二:
【实验分析】
(1)④中发生的两个复分解反应的化学方程式是Na2CO3+2HCl=2NaCl+H2O+CO2↑、Fe2O3+6HCl=2FeCl3+3H2O.

(2)通过实验二可确定固体样品中一定还含有Fe2O3.
(3)为确定固体样品中是否含有氢氧化钙,实验小组同学又经过实验测得上述残留固体总质量为1.66g,滤渣B质量为1.0g,滤渣C的质量为1.0g.
【实验结论】综合上述实验及所给数据,可判断实验小组同学们的猜想成立(填“成立”或“不成立”).
【实验反思】探究硫酸和氢氧化钠反应后硫酸是否有剩余,还可选择一种试剂紫色石蕊试液.
7.下列粒子结构示意图中,表示阴离子的是( )
| A. | 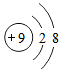 | B. | 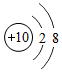 | C. | 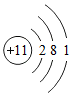 | D. | 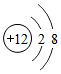 |
17.关于催化剂的说法正确的是( )
| A. | 催化剂只能加快化学反应速率 | |
| B. | 催化剂在化学反应前后其质量和化学性质不变 | |
| C. | 催化剂可增加生成物的量 | |
| D. | 所有化学反应都要使用催化剂 |
1.空气中能供给动植物呼吸的气体是( )
| A. | H2O | B. | O2 | C. | CO2 | D. | N2 |
2.维生素C(化学式C6H8O6)主要存在于蔬菜、水果中,它能促进人体生长发育.下列关于维生素C的说法错误的是( )
| A. | 维生素C由碳元素,氢元素,氧元素组成 | |
| B. | 维生素C中,C、H、O三种元素的质量比为9:1:12 | |
| C. | 维生素C中,氢元素质量分数最小 | |
| D. | 维生素C是由6个碳原子,8个氢原子,6个氧原子构成 |
 化学就在我们身边,它与我们的生活息息相关.
化学就在我们身边,它与我们的生活息息相关.