题目内容
根据图1和图2中A、B两种物质和氢氧化钙的溶解度曲线回答问题.
(1)分析图1,t1℃时,A、B两种物质的溶解度关系为A B(填“>”、“<”或“=”),要使A、B的饱和溶液升高到t2℃,A、B两种物质的溶质质量分数关系为A B(同上).
(2)分析图2,在冬天气温为5℃时配制的氢氧化钙饱和溶液,到了夏天气温为38℃时(水的蒸发不计),可能出现的情况是 (从外观现象、溶质质量分数两方面描述).

(1)分析图1,t1℃时,A、B两种物质的溶解度关系为A
(2)分析图2,在冬天气温为5℃时配制的氢氧化钙饱和溶液,到了夏天气温为38℃时(水的蒸发不计),可能出现的情况是
考点:固体溶解度曲线及其作用,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:根据已有的知识进行分析,根据溶解度曲线即可判断在该温度下两种物质的溶解度关系;氢氧化钙的溶解度随温度的升高而减小.
解答:解:(1)t1℃时,B的溶解度在A的溶解度的上面,A、B两种物质的溶解度关系为A小于B;A、B的饱和溶液升高到t2℃,溶液的组成不变,故溶质质量分数不变,A的小于B,故填:<,<;
(2)氢氧化钙的溶解度随温度的升高而减小,到了夏天,温度升高,则会析出氢氧化钙,导致溶液变浑浊,由于溶质减小,故溶质质量分数变小,故填:溶液变浑浊,溶质质量分数变小.
(2)氢氧化钙的溶解度随温度的升高而减小,到了夏天,温度升高,则会析出氢氧化钙,导致溶液变浑浊,由于溶质减小,故溶质质量分数变小,故填:溶液变浑浊,溶质质量分数变小.
点评:主要考查了对固体溶解度的概念的理解和固体溶解度曲线的意义,以此培养学生的理解能力、培养学生分析问题、解决问题的能力.

练习册系列答案
相关题目
化学学习中接触到的下列说法,符合科学事实的是( )
| A、O2和O3都是由氧元素组成的单质,故由氧元素组成的物质不可能是混合物 |
| B、MnO2、KNO3、CH4O等物质中都含有氧元素,它们都是含氧化合物,都属于氧化物 |
| C、在化合物NO2和N2O4中N元素的化合价均为+4价 |
D、对于反应4NaOH+2S=Na2S+ +2H2O可由质量守恒定律推断出方框内的物质为Na2SO4 +2H2O可由质量守恒定律推断出方框内的物质为Na2SO4 |
20℃时,将等质量不含结晶水的甲、乙固体分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2(不考虑水分蒸发),甲、乙固体的溶解度曲线如图3.下列说法错误的是( )
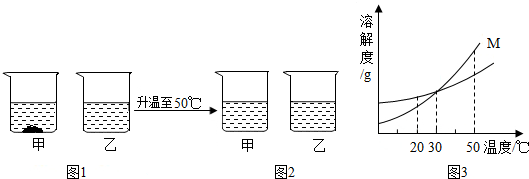

| A、图1中,甲一定是饱和溶液 |
| B、图2中,两溶液中溶质的质量分数一定相等 |
| C、图3中,M表示甲的溶解度曲线 |
| D、图2中,两溶液降温到30℃一定不会析出晶体 |
下列是四位同学分别设计的实验方案,你认为可行的是( )
| A、为除去NaOH溶液的少量Ba(OH)2,先加入适量CuSO4溶液再过滤 |
| B、为检验Zn、Cu、Ag的金属活动性强弱,分别加入稀盐酸中观察气泡产生情况 |
| C、制H2时为减缓反应速率(不影响H2的质量)可向稀H2SO4加入适量的BaCl2溶液 |
| D、为检验纯碱溶液中是否含有烧碱,可先加过量的氯化钙,再加酚酞试液 |
分类是学习化学的方法之一.下列各组物质是按单质、氧化物、混合物的顺序排列的是( )
| A、氧气、水、碘酒 |
| B、氮气、氯酸钾、钢 |
| C、可燃冰、干冰、冰水混合物 |
| D、石墨、熟石灰、石油 |
 回答下列问题:
回答下列问题: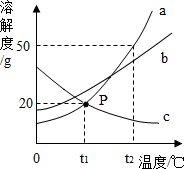 a、b、c三种固体的溶解度曲线如图.
a、b、c三种固体的溶解度曲线如图.