题目内容
5.6g不纯的铁跟足量稀硫酸完全反应后生成0.2g氢气,则样品中一定含有( )
| A、镁 | B、锌 | C、碳 | D、碳和镁 |
考点:金属的化学性质,根据化学反应方程式的计算
专题:金属与金属材料
分析:根据二价金属与酸反应的化学方程式来计算金属的平均相对原子质量,使平均相对原子质量介于56和另一种金属的相对原子质量之间.
解答:解:把不纯的铁看作纯二价金属M,设其相对原子质量为X,则
M+H2SO4═MSO4+H2↑
X 2
5.6g 0.2g
则
=
,解得X═56.
A、镁的相对原子质量为24≠56,若含有镁时,生成的氢气大于0.2g,故A错误.
B、锌的相对原子质量为65>56,若含有锌时,生成的氢气小于0.2g,故B错误.
C、碳不与稀硫酸反应,若含有碳时,只有铁反应,根据化学方程式,5.60g不纯的铁全部反应生成小于0.20g氢气,故C错误.
D、若含有碳和镁,生成的氢气可能等于0.2g,故D正确.
故选:D.
M+H2SO4═MSO4+H2↑
X 2
5.6g 0.2g
则
| X |
| 5.6g |
| 2 |
| 0.2g |
A、镁的相对原子质量为24≠56,若含有镁时,生成的氢气大于0.2g,故A错误.
B、锌的相对原子质量为65>56,若含有锌时,生成的氢气小于0.2g,故B错误.
C、碳不与稀硫酸反应,若含有碳时,只有铁反应,根据化学方程式,5.60g不纯的铁全部反应生成小于0.20g氢气,故C错误.
D、若含有碳和镁,生成的氢气可能等于0.2g,故D正确.
故选:D.
点评:本题考查了学生应用化学方程式计算判断金属的成分,注意利用平均值的方法来解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列化学方程式符合题意且书写正确且基本类型正确的( )
| A、正常雨水呈酸性的原因:CO2+H2O═H2CO3化合反应 | ||||
| B、医疗上用碱性物质中和过多胃酸:Na2CO3+2HCl═2NaCl+CO2↑+H2O 中和反应 | ||||
C、葡萄糖在体内被氧化:12O2+C12H22O11
| ||||
| D、用氢氧化钠溶液检验二氧化碳 CO2+2NaOH═Na2CO3+H2O 复分解反应 |
下列物质中,属于溶液的是( )
| A、米粥 | B、白酒 | C、牛奶 | D、蒸馏水 |
某粒子的结构示意图如图所示,对该粒子的说法错误的是( )


| A、核外电子数为12 |
| B、该粒子的结构示意图为离子结构示意图 |
| C、最外层电子数为2 |
| D、该粒子所形成的离子其符号为Mg2+ |
下列物质的变化中没有发生化学变化的是( )
| A、可乐受热冒出大量气泡 |
| B、一定条件下石墨变成金刚石 |
| C、绿色植物在阳光下进行光合作用 |
| D、水放进冰箱一段时间后结成了冰 |
下列物质的化学式书写错误的是( )
| A、氯化钠 NaCl |
| B、氧化铝 AlO |
| C、氢氧化铁 Fe(OH)3 |
| D、硫酸铜 CuSO4 |
化学科学的发展促进了人类社会文明的进步,化学已日益渗透到社会生活的各个方面.你认为下列各项不属于化学学科基本观念的是( )
| A、物质变化的观念 |
| B、物质运动的观念 |
| C、物质都是由元素组成的观念 |
| D、物质都是由微小粒子构成的观念 |
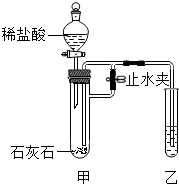 某化学小组在课外活动时做了一个实验,在甲试管中装入固体物质,乙试管中装入试剂溶液,按如图所示组装好仪器(图中铁架台等仪器已略去).通过分液漏斗加入足量稀盐酸,同时打开止水夹,看到乙试管液体中有气泡冒出;再关闭止水夹,发现-段时间后乙中溶液变浑浊.符合此实验现象的是( )
某化学小组在课外活动时做了一个实验,在甲试管中装入固体物质,乙试管中装入试剂溶液,按如图所示组装好仪器(图中铁架台等仪器已略去).通过分液漏斗加入足量稀盐酸,同时打开止水夹,看到乙试管液体中有气泡冒出;再关闭止水夹,发现-段时间后乙中溶液变浑浊.符合此实验现象的是( )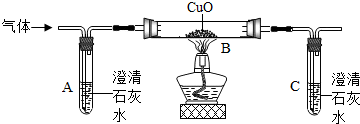 不少同学都被蚊虫叮咬过,感觉又痛又痒.同学们从化学课上知道:蚊虫叮咬时能在人的皮肤内释放出蚁酸刺激皮肤,课外兴趣小组同学决定对蚁酸进行探究.
不少同学都被蚊虫叮咬过,感觉又痛又痒.同学们从化学课上知道:蚊虫叮咬时能在人的皮肤内释放出蚁酸刺激皮肤,课外兴趣小组同学决定对蚁酸进行探究.