题目内容
1.乙酸乙酯(化学式为C4H8O2)常用作食品、饮料的调香剂.请回答下列问题:(1)乙酸乙酯由3种元素组成.
(2)一个乙酸乙酯分子中,碳、氢、氧三种原子的个数比为2:4:1(最简整数比).
(3)乙酸乙酯中碳元素的质量分数为54.5%(计算结果精确到0.1%).
分析 (1)根据化学式可知物质的元素组成;
(2)根据乙酸乙酯可知分子中原子个数比;
(2)根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析判断.
解答 解:(1)乙酸乙酯(化学式为C4H8O2),可知乙酸乙酯由碳、氢、氧三种元素组成;
(2)乙酸乙酯(化学式为C4H8O2),可知一个乙酸乙酯分子中含有4个碳原子、8个氢原子、2个氧原子,故碳、氢、氧原子个数比为:4:8:2=2:4:1;
(3)其中碳元素的质量分数为:$\frac{12×4}{12×4+1×8+16×2}$×100%≈54.5%;
故答案为:(1)3; (2)2:4:1; (3)54.5%.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.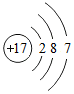 如图是某粒子如图是某粒子的结构示意图,下列说法正确的是( )
如图是某粒子如图是某粒子的结构示意图,下列说法正确的是( )
 如图是某粒子如图是某粒子的结构示意图,下列说法正确的是( )
如图是某粒子如图是某粒子的结构示意图,下列说法正确的是( )| A. | 该粒子的相对原子质量为17 | B. | 该粒子是阴离子 | ||
| C. | 该粒子核外有四个电子层 | D. | 该粒子在化学反应中易得到电子 |
6.由Na2S.Na2SO3.Na2SO4组成的混合物中,测得氧的质量分数为22%.则其中钠的质量分数为( )
| A. | 23% | B. | 46% | C. | 48% | D. | 66% |
13.下列关于日常生产、生活的做法和环境的叙述均正确并有因果关系的是( )
| 日常生产、生活的做法 | 环境 | |
| A | 限制使用含磷洗衣粉 | 磷元素过多会引起水体富营养化,形成赤潮 |
| B | 可以大量使用煤、石油和天然气等化石燃料 | 化石燃料燃烧会过量排放CO2,形成酸雨 |
| C | 可以大量使用塑料制品 | 塑料制品太多会造成白色污染 |
| D | 合理使用化肥、农药 | 过多化肥、农药才能杀死害虫 |
| A. | A | B. | B | C. | C | D. | D |
10.下列环境问题与塑料制品的大量使用和废弃有关的是( )
| A. | 酸雨 | B. | 白色污染 | C. | 臭氧层破坏 | D. | 温室效应 |
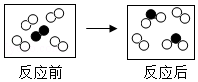 如图是某化学反应的微观示意图,其中“○”和“●”表示不同元素的原子.该反应所属的基本类型为化合反应,参加反应的两种分子个数比为2:1,分析这个反应的微观示意图,总结得出化学反应过程中的一条结论在化学变化中,分子可以再分原子不可再分.
如图是某化学反应的微观示意图,其中“○”和“●”表示不同元素的原子.该反应所属的基本类型为化合反应,参加反应的两种分子个数比为2:1,分析这个反应的微观示意图,总结得出化学反应过程中的一条结论在化学变化中,分子可以再分原子不可再分.