题目内容
20.硫酸铜和硫酸锌混合溶液中加入一定量的铁粉,设计实验,探究反应后溶液中溶质的成分.分析 铁比铜活泼,能和硫酸铜反应生成铜和硫酸亚铁,铁不如锌活泼,所以铁不能和硫酸锌反应;若铁不足,则滤液中溶质是硫酸铜、硫酸亚铁和硫酸锌;若铁恰好反应,则溶液中溶质是硫酸亚铁和硫酸锌;若铁过量,则溶液中溶质是硫酸亚铁和硫酸锌.因此溶液中一定有硫酸亚铁和硫酸锌,关键是检验一下有无硫酸铜.
解答 解:铁比铜活泼,能和硫酸铜反应生成铜和硫酸亚铁,铁不如锌活泼,所以铁不能和硫酸锌反应;若铁不足,则滤液中溶质是硫酸铜、硫酸亚铁和硫酸锌;若铁恰好反应,则溶液中溶质是硫酸亚铁和硫酸锌;若铁过量,则溶液中溶质是硫酸亚铁和硫酸锌.因此溶液中一定有硫酸亚铁和硫酸锌,关键是检验一下有无硫酸铜.取反应后的溶液少许,将铁丝伸入溶液中,若铁丝表面析出红色金属,则溶液中有硫酸铜、硫酸亚铁和硫酸锌,否则只有硫酸亚铁和硫酸锌.
故填:取反应后的溶液少许,将铁丝伸入溶液中,若铁丝表面析出红色金属,则溶液中有硫酸铜、硫酸亚铁和硫酸锌,否则只有硫酸亚铁和硫酸锌.
点评 本题考查了金属活动性顺序的应用,知道排在前面的金属可以把排在后面的金属从其盐溶液中置换出来;氢前金属能与酸反应.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.下列物质按混合物、氧化物、单质顺序进行分类的是( )
| A. | 生理盐水 干冰 液氧 | B. | 石灰石 熟石灰 金刚石 | ||
| C. | 冰水共存物 铁锈 氮气 | D. | 空气 五氧化二磷 生铁 |
15.下列实验目的对应的实验方法正确的是( )
| A. | 比较铜和银的金属活动性分别将铜丝和银丝放入稀盐酸中,观察现象 | |
| B. | 除去CO2中的少量CO点燃混合气体 | |
| C. | 鉴别二氧化碳、氧气和空气将燃着的木条分别伸入瓶中,观察现象 | |
| D. | 比较空气和呼出气体中CO2的含量将燃着的木条分别伸入瓶中,观察现象 |
12.水质好坏直接影响人的健康,高铁酸钾(K2FeO4)是一种新型高效净水处理剂,高铁酸钾是暗紫色粉末,溶于水中生成紫红色溶液,下列有关高铁酸钾的分析中,正确的是( )
| A. | 高铁酸钾是由三种元素组成 | B. | 高铁酸钾中铁元素的化合价是+3价 | ||
| C. | 高铁酸钾是一种氧化物 | D. | 高铁酸钾中含有单质铁 |
9.下列叙述正确的是( )
| A. | 能与碱作用生成盐和水的物质不一定是酸 | |
| B. | 酸的溶液显酸性,碱溶液显碱性,盐的溶液一定显碱性 | |
| C. | 碱都能使酚酞变红 | |
| D. | 复分解反应能否发生与金属的活动性无关 |
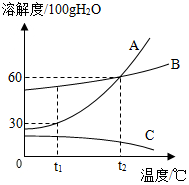 如图是A、B、C三种物质的溶解度曲线,请根据图回答:
如图是A、B、C三种物质的溶解度曲线,请根据图回答: