题目内容
小张同学为了制作叶脉书签,打算配制125g10%的NaOH溶液.
(1)计算小青需要称取NaOH的质量.
(2)小张将洗净的树叶放在配制好的溶液中煮沸后取出,溶液的质量减少了5g,溶质质量分数也有所减小.为了侧定剩下溶液中NaOH的质量分数,小青向溶液中逐渐加入7.3%的稀盐酸,当溶液PH=7时,消耗盐酸50g.计算:
①生成NaCl的质量.
②与盐酸反应的NaOH质量
③剩下溶液中NaOH的质量分数.
| (1)利用溶液中溶质质量=溶液质量×溶液的溶质质量分数,计算125g10%的NaOH溶液中所含溶质氢氧化钠的质量; (2)根据氢氧化钠与盐酸反应的化学方程式,由加入盐酸中HCl的质量计算消耗氢氧化钠的质量和生成氯化钠的质量,氢氧化钠与剩下溶液120g的质量比可计算剩下溶液中NaOH的质量分数. | |
| 解答: | 解:(1)125g10%的NaOH溶液中所含溶质氢氧化钠的质量=125g×10%=12.5g (2)设生成氯化钠的质量为x,参加反应的氢氧化钠的质量为y NaOH+HCl═H2O+NaCl 40 36.5 58.5 y 50g×7.3% x 根据: 氢氧化钠的质量分数= 故答案为:(1)需要称取NaOH的质量12.5g;(2)①生成NaCl的质量5.85g;②与盐酸反应的NaOH质量是4g;③剩下溶液中NaOH的质量分数为3.3%. |

练习册系列答案
相关题目
 解得y=4g,根据
解得y=4g,根据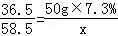 解得 x=5.85g
解得 x=5.85g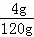 ×100%=3.3%
×100%=3.3%