题目内容
某研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200g,平均分成4等份进行实验,结果如下表:
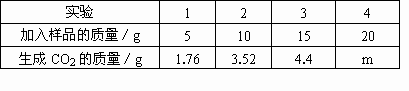
(1)哪几次反应中矿石有剩余?
(2)上表中m的数值是________?
(3)试计算该石灰石矿中碳酸钙的质量分数.
答案:
解析:
提示:
解析:
|
解答:(1)第3、4次反应中矿石有剩余 (2)m=4.4 (3)设矿石中CaCO3的质量为x CaCO3+2HCl=CaCl2+H2O+CO2↑ 100 44 x 1.76g x= 矿石中CaCO3的质量分数: |
提示:
|
点悟:该题需由实验数据中找出规律,然后再依据化学方程式进行计算.从试验中观察到当矿石依次增加5g时,1、2次试验数据间CO2质量增加(3.52-1.76)g=1.76g,而2、3次试验数据间CO2质量增加了(4.4-3.52)g=0.88g,这意味着从第三次起虽然矿石量仍然增加了5g,但CO2的质量并没有增加1.76g,只能是由于稀盐酸的量不足也就是15g矿石没消耗完的结果.因此可知第四次产生CO2的质量m应与第三次相同.求矿石中CaCO3的质量时,需找出完全反应的CaCO3与CO2的关系.由于第2次试验时,随着矿石量的增加,产生CO2的质量也增加,说明第一次试验时5g矿石中的CaCO3完全反应并产生了1.76g CO2. |

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目