题目内容
4.为探究NaOH的性质,某同学进行如下实验:称取4gNaOH固体,放置一段时间,再次称量,质量变为4.2g,将其配成溶液并设计了几种不同的方法来分析NaOH是否变质.该同学做法及判断正确的是( )| A. | 根据固体质量的增加,说明NaOH已发生变质 | |
| B. | 取少量液体,滴入稀硫酸,有气泡产生,说明NaOH已发生变质 | |
| C. | 取少量液体,滴入硫酸铜溶液,产生蓝色沉淀,说明NaOH没有变质 | |
| D. | 取少量液体,滴入无色酚酞试液,溶液变为红色,说明NaOH没有变质 |
分析 A、根据氢氧化钠固体有吸水性进行分析;
B、根据氢氧化钠变质生成的碳酸钠和硫酸反应会生成二氧化碳气体进行分析;
C、根据氢氧化钠部分变质和硫酸铜反应也会生成氢氧化铜沉淀进行分析;
D、根据氢氧化钠和碳酸钠都显碱性,都能是酚酞变红色进行分析.
解答 解:A、氢氧化钠固体有吸水性,所以固体质量的增加,不能说明NaOH已发生变质,故A错误;
B、氢氧化钠变质生成的碳酸钠和硫酸反应会生成二氧化碳气体,所以取少量液体,滴入稀硫酸,有气泡产生,说明NaOH已发生变质,故B正确;
C、氢氧化钠部分变质和硫酸铜反应也会生成氢氧化铜沉淀,故C错误;
D、氢氧化钠和碳酸钠都显碱性,都能是酚酞变红色,故D错误.
故选:B.
点评 本题主要考查了氢氧化钠和碳酸钠的性质,难度不大,需要在平时的学习中加强记忆.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
14.下列关于化肥和农药的说法错误的是( )
| A. | 尿素[CO(NH4)2]是一种氮肥 | |
| B. | 化肥对提高农作物产量有重要作用 | |
| C. | 农药本身有毒,应该禁止使用 | |
| D. | 目前施用农药仍是最重要的作物保护手段 |
15.关于太阳能路灯的说法不正确的是( )


| A. | 铝合金灯柱属于金属材料 | |
| B. | 灯泡中填充氮气作保护气 | |
| C. | 透明的塑料灯罩属于有机合成高分子材料 | |
| D. | 硅电池板中的硅元素是地壳中含量最多的元素 |
12.如图所示实验操作中正确的是( )
| A. |  氧气验满 | B. | 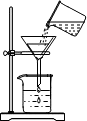 过滤 | ||
| C. | 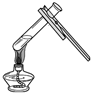 给液体加热 | D. | 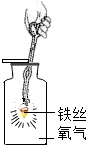 铁丝在氧气中燃烧 |
19.实验室几种液体的pH如表(室温下):
参考以上数据分析下列推论正确的是( )
| 液体 | 盐酸 | CuSO4溶液 | NaCl溶液 | 水 | Na2CO3溶液 | NaOH溶液 |
| pH | <7 | <7 | =7 | =7 | >7 | >7 |
| A. | pH>7的液体一定是碱溶液 | B. | pH<7的液体一定是酸溶液 | ||
| C. | pH=7的液体一定是盐溶液 | D. | 盐溶液可能显酸性、碱性或中性 |
9.汽车在受到猛烈撞击时安全气囊内的物质瞬间分解,产生的是空气中体积分数最大的气体.该气体是( )
| A. | 氮气 | B. | 氧气 | C. | 氦气 | D. | 水蒸气 |
13.下列化学反应,属于复分解反应的是( )
| A. | C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ | B. | 2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑ | ||
| C. | C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O | D. | Na2CO3+Ca(OH)2═CaCO3↓+2NaOH |
3.一氧化氮是一种大气污染物,它是一种难溶于水,密度比空气的密度略大,在空气中能与氧气迅速反应生成二氧化氮气体.在实验室中收集一氧化氮的方法是( )
| A. | 排水法 | B. | 向上排空气法 | ||
| C. | 向下排空气法 | D. | 排水集气法或向上排空气法 |
