题目内容
15.CO是冶金工业常用的还原剂,用于冶炼金属.观察下列反应,寻找规律,CO+FeO$\frac{\underline{\;高温\;}}{\;}$ Fe+CO2
3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$ 2Fe+3CO2
4CO+Fe3O4 $\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2
若用CO还原FexOy,则可推知化学方程式中CO2的化学计量数(即化学式前边的系数)为y.
分析 根据提供的三个化学方程式,可以看出,一个CO分子反应中获得一个氧原子变为二氧化碳分子,铁的氧化物失去氧原子的个数即为一氧化碳前面的化学计量数,据此进行分析解答.
解答 解:由提供的三个化学方程式,可以看出,一个CO分子反应中获得一个氧原子变为二氧化碳分子,铁的氧化物失去氧原子的个数即为一氧化碳前面的化学计量数;故
用CO还原FexOy,可从得失氧的角度配平,一个CO分子反应中获得一个氧原子变为二氧化碳分子,由于一个FexOy分子中氧原子的数目为y个,所以CO与CO2前面的化学计量数都为y,最后配平其它元素的原子,FexOy、Fe前面的化学计量数分别为1、x.
故答案为:y.
点评 本题难度不大,掌握化学反应前后各原子的数目不变、化学方程式的配平方法等是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.科学探究是奇妙的过程,某同学在进行实验探究时,向一种无色液体中加入一种银白色金属固体,立即产生一种无色无味的体.
①此气体是什么物质?验证它的实验方案如下:
②产生此气体的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑.可用向上排空气(填下序号)法收集该气体.
③该同学想制取该气体,现提供制取和收集该气体的装置如图所示,请你帮他选择.
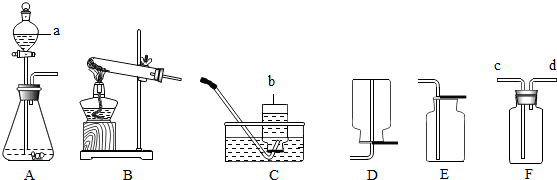
A.若要制取并收集该气体,应采用的发生装置、收集装置分别是A、E(填序号).利用该发生装置实验室还可以制取O2气体(填气体的化学式).
C.若用图F收集该气体,气体应从c端(填“c”或“d”)导人.
①此气体是什么物质?验证它的实验方案如下:
| 猜想 | 实验步骤 | 现象及结论 |
| 此气体可能是CO2 | 将产生的气体通入澄清石灰水中 | 变浑浊则猜想成立 |
③该同学想制取该气体,现提供制取和收集该气体的装置如图所示,请你帮他选择.

A.若要制取并收集该气体,应采用的发生装置、收集装置分别是A、E(填序号).利用该发生装置实验室还可以制取O2气体(填气体的化学式).
C.若用图F收集该气体,气体应从c端(填“c”或“d”)导人.
3.卢瑟福α粒子散射实验的结果( )
| A. | 证明了质子的存在 | |
| B. | 证明了原子核是由质子和中子组成的 | |
| C. | 证明了原子核的全部正电荷和几乎全部质量都集中在一个很小的核上 | |
| D. | 说明原子中的电子只能在某些不连续的轨道上运动 |
10.下列物质属于纯净物的是 ( )
| A. | 生铁 | B. | 黄铜 | C. | 不锈钢 | D. | 干冰 |
4.鉴别高锰酸钾、食盐和二氧化锰三种试剂最简单的方法是( )
| A. | 加热法 | B. | 溶解法 | C. | 称量法 | D. | 观察法 |
5.学习了MnO2对过氧化氢分解有催化作用的知识后,某同学想:氧化铜(CuO)能否起到类似MnO2的催化作用呢?于是进行了以下探究.
【猜想】
Ⅰ.CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ.CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ.CuO是反应的催化剂,反应前后质量和化学性质不变.
【实验】用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如图1的实验:
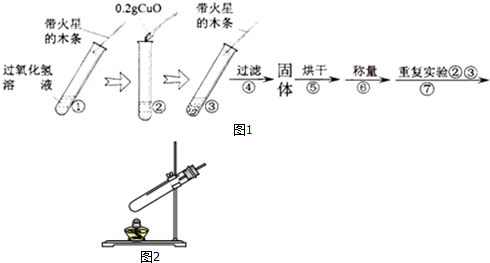
(1)填写下表:
(2)步骤①(填序号)的目的是证明CuO能加快过氧化氢溶液分解的速率;
(3)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、玻璃棒.
(4)步骤⑦的目的是证明氧化铜的化学性质在反应前后没有发生改变.
(5)过氧化氢能被CuO催化分解放出O2的文字表达式为过氧化氢$\stackrel{氧化铜}{→}$水+氧气.
(6)同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以产生氧气,同学们选择如图2装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是氧气中混有较多的水蒸气,同学分析原因后,采用了排水法收集气体,再检验,证明加热双氧水也可产生氧气.
【猜想】
Ⅰ.CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ.CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ.CuO是反应的催化剂,反应前后质量和化学性质不变.
【实验】用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如图1的实验:

(1)填写下表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 剧烈反应,产生大量气泡 带火星的木条复燃 | 0.2g | 溶液中有气泡放出 带火星木条复燃 | 猜想Ⅰ、Ⅱ不成立 猜想Ⅲ成立 |
(3)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、玻璃棒.
(4)步骤⑦的目的是证明氧化铜的化学性质在反应前后没有发生改变.
(5)过氧化氢能被CuO催化分解放出O2的文字表达式为过氧化氢$\stackrel{氧化铜}{→}$水+氧气.
(6)同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以产生氧气,同学们选择如图2装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是氧气中混有较多的水蒸气,同学分析原因后,采用了排水法收集气体,再检验,证明加热双氧水也可产生氧气.