题目内容
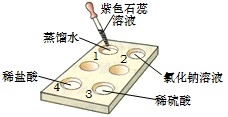
 24、盐酸溶液中含有H2O分子、H+和Cl-离子,要探究是哪一种粒子能使紫色石蕊溶液变成红色,请观察在白色点滴板上进行的下列实验,将实验现象和结论填入下表.
24、盐酸溶液中含有H2O分子、H+和Cl-离子,要探究是哪一种粒子能使紫色石蕊溶液变成红色,请观察在白色点滴板上进行的下列实验,将实验现象和结论填入下表.| 滴加紫色石蕊溶液后的现象 | 结论 | |
| 第1孔 | 孔中溶液为紫色 | 水分子不能使紫色石蕊试液变成红色 |
| 第2孔 | 孔中溶液为紫色 |
Cl-离子不能使紫色石蕊试液变成红色 |
| 第3孔、第4孔 | 孔中溶液为红色 |
H+离子使紫色石蕊试液变成红色 |
分析:蒸馏水中只含有水分子,滴加紫色石蕊试液不变色,说明水分子不能使紫色石蕊试液变成红色;氯化钠溶液中含有Cl-离子,滴加紫色石蕊试液不变色,说明Cl-离子也不能使紫色石蕊试液变成红色;盐酸溶液中含有H2O分子、H+和Cl-离子,能使紫色石蕊试液变成红色,排除水分子、Cl-离子,从而可以说明H+离子使紫色石蕊试液变成红色.
解答:解:蒸馏水中滴加紫色石蕊试液不变色,说明水分子不能使紫色石蕊试液变成红色;氯化钠溶液显中性,不能使紫色石蕊试液变色,所以孔中溶液为紫色,可以得出Cl-离子不能使紫色石蕊试液变成红色的结论;排除了水分子、Cl-离子之后可以得出H+离子使紫色石蕊试液变成红色的结论,所以第3、4孔中溶液为红色的现象.
故答案为水分子不能使紫色石蕊试液变成红色;孔中溶液为紫色;Cl-离子不能使紫色石蕊试液变成红色;孔中溶液为红色;H+离子使紫色石蕊试液变成红色.
故答案为水分子不能使紫色石蕊试液变成红色;孔中溶液为紫色;Cl-离子不能使紫色石蕊试液变成红色;孔中溶液为红色;H+离子使紫色石蕊试液变成红色.
点评:酸性溶液能使紫色石蕊试液变红,使无色酚酞试液不变色,是因为酸中都含有H+离子;碱性溶液能使紫色石蕊试液变蓝,使无色酚酞试液变红,是因为碱性溶液中都含有OH-离子.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
(2010?昆明)盐酸溶液中含有H2O分子、H+和Cl-离子,要探究是哪一种粒子能使紫色石蕊溶液变成红色,请观察在白色点滴板上进行的下列实验,将实验现象和结论填入下表.

| 滴加紫色石蕊溶液后的现象 | 结论 | |
| 第1孔 | 孔中溶液为紫色 | ______ |
| 第2孔 | ______ | ______ |
| 第3孔、第4孔 | ______ | ______ |