题目内容
20. 通过学习金属的知识,同学们知道了可用酸来鉴别黄金和黄铜(铜锌合金,俗名“愚人金”).某同学为进一步分析黄铜的成分,称量黄铜样品20g放入锥形瓶中,向其中不断加入稀硫酸,收集生成的气体与所加稀硫酸的质量关系如图所示.试计算:
通过学习金属的知识,同学们知道了可用酸来鉴别黄金和黄铜(铜锌合金,俗名“愚人金”).某同学为进一步分析黄铜的成分,称量黄铜样品20g放入锥形瓶中,向其中不断加入稀硫酸,收集生成的气体与所加稀硫酸的质量关系如图所示.试计算:(1)黄铜样品中锌的质量分数.
(2)所用硫酸的溶质质量分数.
分析 (1)黄铜中的锌能够和稀硫酸反应,根据反应生成的氢气可以计算出黄铜样品中的锌的质量,然后求算出其质量分数即可;
(2)根据化学方程式结合氢气的质量计算出硫酸的质量,进而求出其质量分数即可.
解答 解:由图中可以知道生成氢气的质量为0.2g
设锌的质量为x,硫酸的质量为y
Zn+H2SO4═ZnSO4+H2↑
65 98 2
x y 0.2g
$\frac{65}{x}$=$\frac{98}{y}$=$\frac{2}{0.2g}$
解得:x=6.5g y=9.8g
(1)黄铜样品中锌的质量分数为:$\frac{6.5g}{20g}$×100%=32.5%.
(2)所用硫酸的溶质质量分数为:$\frac{9.8g}{154g}$×100%=6.4%
答:(1)黄铜样品中锌的质量分数为32.5%.
(2)所用硫酸的溶质质量分数为6.4%.
点评 本题主要考查了利用化学方程式进行计算,难度不大,需要弄清应用的原理,然后结合题中的数据即可解答.

练习册系列答案
相关题目
10.具备基本的化学实验技能是进行科学探究的基础和保证.下列操作正确的是( )
| A. | 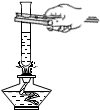 加热反应物 | B. | 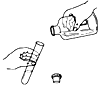 倾倒液体 | C. | 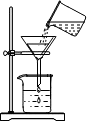 过滤 | D. |  读取液体体积 |
11.下列各种物质的名称、俗称和化学式表示的是同一种物质的是( )
| A. | 氢氧化钙,熟石灰,CaCO3 | B. | 氢氧化钠,烧碱,NaOH | ||
| C. | 氯化钠,纯碱,NaCl | D. | 氧化钙,石灰水,Ca(OH)2 |
8.金属、金属材料的性质在很大程度上决定了它们的用途.下列说法中不正确的是( )
| A. | 不锈钢抗腐蚀性好,常用语制造医疗器械 | |
| B. | 铁具有良好的导热性,可以用于制造炊具 | |
| C. | 钛合金与人体具有很好的“相容性”,常用来制造人造骨 | |
| D. | 银具有很好的导电性,常用于制电线 |
5.如图是某反应的微观示意图,依据此图判断下列说法正确的是( )
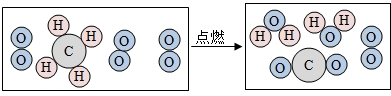

| A. | 该反应的生成物中都是化合物 | |
| B. | 该反应中反应物各物质的粒子个数比是1:3 | |
| C. | 从微观的角度看该反应前后分子种类和原子个数都不变 | |
| D. | 从微观的角度看该反应还能体现出分子可以再分,原子也可以再分 |
12.小东同学本学期的化学知识作了一些归纳与整理笔记,林老师对笔记进行检查发现了一些问题,列举了几例,请仿照示例在“判断与解释”栏中回答有关问题.
| 归纳与整理 | 判断与解释 |
| 例1:物质与氧气发生的化合反应都是氧化反应. | 正确 |
| 例2:所有的原子核内都有质子、中子. | 不正确,如:H的原子核内没有中子 |
| 练1:一种元素组成的物质一定是单质. | 不正确,如金刚石和石墨一种元素形成的混合物 |
| 练2:可燃物在水下也可以燃烧. | 正确 |
| 练3:固体物质的饱和溶液降低温度一定析出晶体. | 不正确,如熟石灰的饱和溶液降低温度就无晶体析出 |
9.善于归纳和总结是科学的学习方法,下列归纳总结正确的是( )
| A. | 化石燃料:煤、石油、天然气 | B. | 单质:水、石墨、氦气 | ||
| C. | 天然纤维:塑料、纤维、橡胶 | D. | 碱:烧碱、熟石灰、纯碱 |
10.下列变化中,属于化学变化的是( )
| A. | 汽油挥发 | B. | 水的电解 | ||
| C. | 瓷碗破碎 | D. | 将液态空气分离制得氧气 |