题目内容
8.下列反应中,不属于化合、分解、置换、复分解等四种基本反应类型的是( )| A. | CuSO4+H2S═CuS↓+H2SO4 | B. | Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+CO2↑+H2O | ||
| C. | 2FeCl3+Cu═2FeCl2+CuCl2 | D. | 4Fe(OH)2+O2+2H2O═4Fe(OH)3 |
分析 化合反应指的是由两种或两种以上的物质生成一种新物质的化合反应;
分解反应是指一种化合物在特定条件下,分解成二种或二种以上较简单的单质或化合物的反应;
复分解反应指由两种化合物互相交换成分,生成另外两种化合物的反应;
置换反应是一种单质与一种化合物反应生成另外的一种单质和另外一种化合物的化学反应.
解答 解:A.该反应由两种化合物相互交换成分生成另外的化合物,为复分解反应,故A不选;
B.该反应由一种物质生成三种物质,为分解反应,故B不选;
C.该反应由一种单质和一种化合物反应生成另外的两种化合物,不属于化合、分解、置换、复分解等四种基本反应类型,但属于氧化还原反应,故C选;
D.该反应由三种物质生成一种物质,为化合反应,故D不选;
故选C.
点评 本题考查了化学基本反应类型的判断,明确这四个概念的内涵是解本题关键,根据概念来判断即可,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.“侯氏制碱法”是我国近代著名科学家侯德榜发明的一种连续生产纯碱与氯化铵的联合制碱工艺,同学们查阅相关资料并进行模拟实验.
【查阅资料】
①生产原理:NaCl(饱和溶液)+NH3+CO2+H2O=NaHCO3(固体)↓+NH4Cl
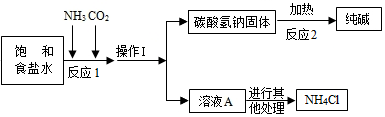
②主要生产流程如图所示:
③氨气(NH3)是一种有刺激性气味的气体,极易溶于水,其水溶液显碱性.
【理论分析】
(1)依据资料①可知相同条件下,NaHCO3的溶解度NH4Cl的溶解度<(填“>”或“<”).
(2)NaHCO3受热分解制得纯碱及两种常见的氧化物,该反应的化学方程式是2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
【模拟实验】验证侯氏制碱法能获得纯碱
【实验反思】同学们认为步骤3的结论存在不足.依据题中信息,设计实验确定步骤2加热后得到的固体成分,其方案是将生成的气体通入澄清的石灰水,观察到澄清的石灰水变浑浊,证明步骤2加热后得到的是碳酸氢钠.
【查阅资料】
①生产原理:NaCl(饱和溶液)+NH3+CO2+H2O=NaHCO3(固体)↓+NH4Cl
②主要生产流程如图所示:

③氨气(NH3)是一种有刺激性气味的气体,极易溶于水,其水溶液显碱性.
【理论分析】
(1)依据资料①可知相同条件下,NaHCO3的溶解度NH4Cl的溶解度<(填“>”或“<”).
(2)NaHCO3受热分解制得纯碱及两种常见的氧化物,该反应的化学方程式是2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
【模拟实验】验证侯氏制碱法能获得纯碱
| 步骤 | 蘸有稀硫酸 实验装置 | 实验操作及现象 | 解释与结论 |
| 1 | 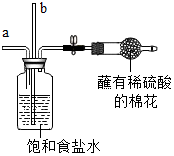 | 从a管通入NH3,一段时间后,从b管通入CO2,溶液中有固体析出 | (1)蘸有稀硫酸的棉花的作用是 (2)通NH3的a管若伸到液面下,会造成的后果是 |
| 2 | 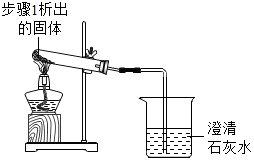 | 加热,导管口有气泡,澄清石灰水变浑浊 | 步骤1析出的固体是碳酸氢钠 |
| 3 | 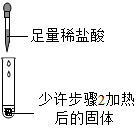 | 滴加足量稀盐酸,有气泡产生,固体逐渐消失 | 步骤2加热后得到的固体是纯碱 |
19.下列化学用语表述,属于科学规范的是( )
| A. | 氯酸钾分解的化学方程式:2KclO3$\frac{\underline{\;MnO_{2}\;}}{\;}$2KCl+3O2 | |
| B. | 氧离子的符号:O22- | |
| C. | 镁原子的结构示意图: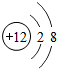 | |
| D. | 碱式碳酸镁的化学式:Mg2(OH)2CO3 |
13.由FeSO4和Fe2(SO4)3组成的混合物中,含硫为a%,则所含铁的质量百分含量为( )
| A. | 3a% | B. | (100-2a)% | C. | 20% | D. | 1-3a% |
20.下列变化中,属于化学变化的是( )
| A. | 瓷碗破碎 | B. | 石蜡熔化 | C. | 玉米酿酒 | D. | 汽油挥发 |