题目内容
20.化学与社会、人类生活密切相关,下列归纳错误的一项是( )| A. | 化学与安全:重金属中毒--喝鲜牛奶、豆浆等解毒;煤气泄漏--关闭气阀,严禁烟火 | |
| B. | 化学与生活:水中有异味--用活性炭吸附;鉴别纯棉织物和纯毛织物--灼烧闻气味 | |
| C. | 物理性质与用途:O2可燃--气焊切割金属;纯碱能与盐酸反应--治疗胃酸过多 | |
| D. | 化学与材料:塑料、橡胶--都属于有机高分子材料;生铁、黄铜--都属于金属材料 |
分析 A、根据重金属中毒的原理、煤气属于可燃性气体进行解答;
B、根据活性炭具有吸附性、纯毛织物的主要成分是蛋白质,燃烧后有烧焦羽毛的味道进行解答;
C、根据氧气不具有可燃性、一般用碳酸氢钠能与胃酸反应,治疗胃酸过多症;
D、根据材料的分类进行解答.
解答 解:A、重金属中毒的原理是破坏人体内的蛋白质,而鲜牛奶、豆浆含有蛋白质,所以可喝鲜牛奶、豆浆等解毒;煤气属于可燃性气体,遇明火会发生爆炸,所以煤气泄漏,关闭气阀,严禁烟火,故A正确;
B、活性炭具有吸附性,能吸附水中有异味;纯毛织物的主要成分是蛋白质,燃烧后有烧焦羽毛的味道,所以可用灼烧闻气味鉴别纯棉织物和纯毛织物,故B正确;
C、氧气不具有可燃性,碳酸氢钠能与胃酸反应,治疗胃酸过多症,故C错误;
D、塑料、橡胶都属于有机高分子材料,生铁、黄铜--都属于金属材料,故D正确.
故选:C.
点评 与生产、生活相关的知识是中考考查的热点之一,本题难度不大,但涉及知识点较多,灵活运用所学知识是即可正确解答本题.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
10.下列物质的用途中,利用其物理性质的是( )
| A. | 双氧水作消毒剂 | B. | 铁粉用于食品保存 | ||
| C. | 人造金刚石可作钻探机的钻头 | D. | 用氢氧化钠溶液制作“叶脉书签” |
8.化学影响着社会的发展和人们的生活质量.以下说法正确的是( )
| A. | 为提高农作物产量,应大量施用农药化肥 | |
| B. | 为减少“白色污染”,应尽量使用黑色塑料 | |
| C. | 为使虾能长久保存,应用甲醛溶液浸泡 | |
| D. | 糖类是人体生命活动主要的供能物质 |
9.下列关于“2”的含义的解释中,正确的是( )
| A. | Zn2+中的“2+”表示锌粒带有2个单位的正电荷 | |
| B. | 2NO中的“2”表示2个一氧化氮分子 | |
| C. | H2O中的“2”表示一个水分子中含有二个氢元素 | |
| D. | Al2(SO4)3中的“2”表示硫酸铝中个含有2个铝原子 |
10. 同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?
同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?
在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.
(1)实验准备
①查阅资料:NaHCO3+NaOH═Na2CO3+H2O
Ca(OH)2+Na2CO3═CaCO3↓+2NaOH
CaCl2+2NaOH═Ca(OH)2↓(微溶)+2NaCl
2NaHCO3(溶液)$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑
NaHCO3+HCl═NaCl+H2O+CO2↑
Ca(OH)2+NaHCO3═CaCO3↓+NaOH+H2O
②前期实验:
用一定溶质的质量分数的NaHCO3、NaOH和Na2CO3三种溶液进行如下实验,为设计实验方案提供参考.
Ⅰ对应反应的化学方程式为HCl+NaOH═NaCl+H2O,
Ⅱ的现象为有沉淀产生.
(2)实验过程
【实验1】证明NaOH溶液与NaHCO3溶液反应生成了Na2CO3
同学们选用上表实验中的药品,设计了如图所示实验,先在NaHCO3溶液中加入A溶液,无明显现象,再滴加NaOH溶液,溶液变浑浊,则A溶液是CaCl2.有同学提出这个实验不足以证明有Na2CO3生成,其理由是CaCl2 和NaOH反应生成Ca(OH)2,氢氧化钙是微溶物,在溶液中也产生沉淀.为了证明有Na2CO3生成,需要继续进行的操作是:取少量反应后的滤渣加入足量的取少量反应后滤渣加入足量的稀盐酸,若产生无色气体证明有Na2CO3生成,反之则没有,若产生无色气体证明有Na2CO3生成,反之则没有.
【实验2】证明NaOH溶液与NaHCO3溶液反应后NaHCO3不存在
同学们参考上表中的实验,又设计了一个实验,虽然没有观察到明显的实验现象,但可以证明反应发生了,该实验方案是取少量反应后的溶液进行取少量反应后的溶液加热至沸腾(填操作),将产生的气体通入澄清石灰水,若澄清石灰水变浑浊,证明有NaHCO3存在,反之则没有.
(3)实验反思
通过实验1和实验2说明,对于没有明显现象的化学反应,可以从不同的角度证明反应的发生,比如:一是可以通过反应物检验证明反应发生;二是可以通过产物检验证明反应发生.
 同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?
同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.
(1)实验准备
①查阅资料:NaHCO3+NaOH═Na2CO3+H2O
Ca(OH)2+Na2CO3═CaCO3↓+2NaOH
CaCl2+2NaOH═Ca(OH)2↓(微溶)+2NaCl
2NaHCO3(溶液)$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑
NaHCO3+HCl═NaCl+H2O+CO2↑
Ca(OH)2+NaHCO3═CaCO3↓+NaOH+H2O
②前期实验:
用一定溶质的质量分数的NaHCO3、NaOH和Na2CO3三种溶液进行如下实验,为设计实验方案提供参考.
| NaHCO3溶液 | NaOH溶液 | Na2CO3溶液 | |
| 加入稀盐酸 | 产生气泡 | Ⅰ | 产生气泡 |
| 加入澄清石灰水 | 溶液变浑浊 | 无明显变化 | Ⅱ |
| 加入CaCl2溶液 | 无明显变化 | 溶液变浑浊 | 溶液变浑浊 |
| 加热溶液至沸腾,将 气体通入澄清石灰水 | 澄清石灰水 变浑浊 | 澄清石灰水 无明显变化 | 澄清石灰水 无明显变化 |
Ⅱ的现象为有沉淀产生.
(2)实验过程
【实验1】证明NaOH溶液与NaHCO3溶液反应生成了Na2CO3
同学们选用上表实验中的药品,设计了如图所示实验,先在NaHCO3溶液中加入A溶液,无明显现象,再滴加NaOH溶液,溶液变浑浊,则A溶液是CaCl2.有同学提出这个实验不足以证明有Na2CO3生成,其理由是CaCl2 和NaOH反应生成Ca(OH)2,氢氧化钙是微溶物,在溶液中也产生沉淀.为了证明有Na2CO3生成,需要继续进行的操作是:取少量反应后的滤渣加入足量的取少量反应后滤渣加入足量的稀盐酸,若产生无色气体证明有Na2CO3生成,反之则没有,若产生无色气体证明有Na2CO3生成,反之则没有.
【实验2】证明NaOH溶液与NaHCO3溶液反应后NaHCO3不存在
同学们参考上表中的实验,又设计了一个实验,虽然没有观察到明显的实验现象,但可以证明反应发生了,该实验方案是取少量反应后的溶液进行取少量反应后的溶液加热至沸腾(填操作),将产生的气体通入澄清石灰水,若澄清石灰水变浑浊,证明有NaHCO3存在,反之则没有.
(3)实验反思
通过实验1和实验2说明,对于没有明显现象的化学反应,可以从不同的角度证明反应的发生,比如:一是可以通过反应物检验证明反应发生;二是可以通过产物检验证明反应发生.
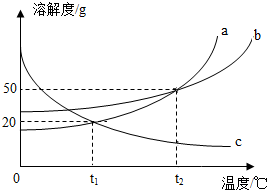 如图是a、b、c三种固体物质(不含结晶水)的溶解度曲线图,根据曲线图回答下列问题.
如图是a、b、c三种固体物质(不含结晶水)的溶解度曲线图,根据曲线图回答下列问题.