题目内容
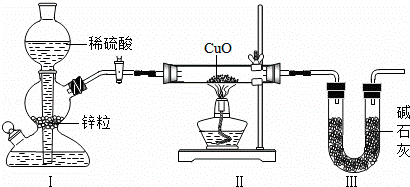
A、B、C、D、E、F、G为常见的物质,其中B、E、G属于单质,反应②是炼铁工业中的主要反应,下图是它们之间的相互转化关系.请回答:
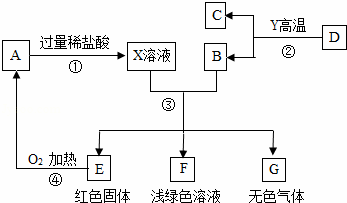
(1)X溶液中所含有的溶质为 ,固体A的化学式为 ,F中显浅绿色的离子的离子符号 .
写出反应②的化学方程式 ,
(3)写出反应③中生成红色固体的化学方程式 ,
(4)上图转化中产生无色气体G的原因是 ,
(5)指出物质G和A在加热条件下发生的化学反应的基本反应类型 .
考点: 化学的研究对象及其发展;溶液、溶质和溶剂的相互关系与判断;金属的化学性质;一氧化碳还原氧化铁;酸的化学性质;化学式的书写及意义;化合价与离子表示方法上的异同点;反应现象和本质的联系;反应类型的判定;书写化学方程式、文字表达式、电离方程式.
专题: 框图型推断题;压轴实验题.
分析: 找出突破口,反应②是炼铁工业中的主要反应,即一氧化碳还原氧化铁生成铁和二氧化化碳,再根据其中B、E、G属于单质,和常见现象的判断:红色固体是铜、浅绿色溶液是亚铁离子溶液.进一步进行推断.
解答: 解:由反应②是炼铁工业中的主要反应,即一氧化碳还原氧化铁生成铁和二氧化化碳,又因为B是单质,所以B是铁,C是二氧化碳;
E是红色固体,可先认为是铜,则A是氧化铜,氧化铜与过量盐酸反应,所以X溶液中会含有盐酸和氯化铜,再和铁反应,铁和盐酸反应生成氯化亚铁和氢气,铁和氯化铜反应生成铜和氯化亚铁,所以E是铜、F是氯化亚铁、G是氢气.
故答案为:(1)氯化铜和氯化氢,CuO,Fe2+;
3CO+Fe2O3 2Fe+3CO2;
2Fe+3CO2;
(3)Fe+CuCl2=Cu+FeCl2;
(4)铁与过量的盐酸反应生成的;
(5)置换反应.
点评: 先根据所提供信息,找出突破口,再根据熟悉的现象进行有依据性的猜测,再进行验证.

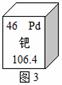 ①汽车尾气处理中使用了催化剂,该催化剂中某元素在元素周期表中的部分内容如图3所示,从中获取一条信息:_______________________________。
①汽车尾气处理中使用了催化剂,该催化剂中某元素在元素周期表中的部分内容如图3所示,从中获取一条信息:_______________________________。