题目内容
5.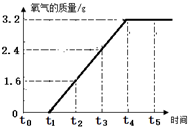 实验室制取氧气时,某同学取质量为x的高锰酸钾加热,记录产生氧气的质量和时间的关系如图所示,请回答下列问题:
实验室制取氧气时,某同学取质量为x的高锰酸钾加热,记录产生氧气的质量和时间的关系如图所示,请回答下列问题:(1)t0-t1时段固体的质量不发生变化是因为反应还未进行;t4-t5时段,固体的质量不发生变化,是因为反应已经结束.
(2)请根据图中的数据,计算高锰酸钾的质量是多少?(写出计算的过程)
(3)t3时,固体中锰元素的质量为11 g.
分析 (1)根据图中信息解答;
(2)根据图1可知,氧气的质量为3.2克,根据氧气的质量,利用氧气的质量根据反应的方程式即可计算出高锰酸钾的质量;
(3)根据质量守恒定律,化学反应前后锰元素的质量不变解答.
解答 解:
(1)根据图中信息可知:t0-t1固体质量不变,是因为反应还未进行;t4-t5时固体质量不变,是因为反应进行完全;
(2)设高锰酸钾的质量是x,由图象可知该反应生成的氧气质量是3.2g;
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
316 32
x 3.2g
$\frac{316}{x}$=$\frac{32}{3.2g}$
x=31.6g
答:高锰酸钾的质量为31.6g.
(3)31.6g高锰酸钾中锰元素的质量是31.6g×$\frac{55}{158}$×100%=11g
故答案为:(1)反应还未进行;反应已经结束.
(2)31.6g
(3)11.
点评 本题为根据化学方程式计算类问题中的基础计算,完整的计算步骤、规律的书写格式是解答此类问题时需要留意的地方.

练习册系列答案
相关题目
15.下列说法错误的是( )
| A. | 在化学变化中分子可以再分,原子不能再分 | |
| B. | 原子失去电子形成阳离子 | |
| C. | 原子核中质子带正电,中子不带电 | |
| D. | 分子能直接构成物质,原子不能 |
16.茶叶中的单宁酸具有抑制血压上升、清热解毒、抗癌等功效,其化学式为C76H52O46.下列说法错误的是( )
| A. | 单宁酸由碳、氢、氧三种元素组成 | |
| B. | 一个单宁酸分子是由76个碳原子、52个氢原子和46个氧原子构成 | |
| C. | 单宁酸中碳、氧元素的质量比为76:46 | |
| D. | 单宁酸中氢元素的质量分数最小 |
13.下列物质的化学式不正确的是( )
| A. | 氦气 He | B. | 氧化镁 OMg | C. | 氧气 O2 | D. | 水 H2O |
20.下列图示实验操作中,正确的是( )
| A. |  滴加液体 | B. | 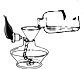 添加酒精 | C. | 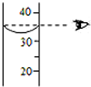 量取液体 | D. | 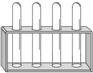 放置试管 |
17.燃烧是物质与氧气发生的剧烈的发光发热的氧化反应,同学们按如图装置对“可燃物燃烧的条件”进行探究.
【查阅资料】白磷的着火点是40℃,红磷的着火点是240℃,燃烧产物五氧化二磷是白色固体,会刺激人体呼吸道,可能与空气中水蒸气反应,生成有毒的偏磷酸(HPO3).
实验过程中的现象是产生大量的白烟,放出大量的热,生成一种白色固体
【交流讨论】白烟对人体健康有害,该实验装置必须改进.
(1)【改进实验】同学们按改进后的如图装置进行实验.

请你帮助他们将下表补充完整.
(2)【反思评价】
改进后的装置比较,优点是能防止白磷燃烧产生的五氧化二磷逸散,危害人体健康
(3)根据白磷着火点低的性质,同学们进一步思考,将测定空气中氧气含量的实验装置改进如图4所示,经过测量,发现空气中氧气含量不足五分之一,可能的原因是红磷的量不足或是装置的气密性不好都会导致集气瓶内的水位上升不足五分之一.
【查阅资料】白磷的着火点是40℃,红磷的着火点是240℃,燃烧产物五氧化二磷是白色固体,会刺激人体呼吸道,可能与空气中水蒸气反应,生成有毒的偏磷酸(HPO3).
实验过程中的现象是产生大量的白烟,放出大量的热,生成一种白色固体
【交流讨论】白烟对人体健康有害,该实验装置必须改进.
(1)【改进实验】同学们按改进后的如图装置进行实验.

请你帮助他们将下表补充完整.
| 现象 | 解释 |
| a试管中白磷燃烧,热水中的白磷没有燃烧; b试管中红磷没有燃烧. | b试管中红磷、热水中白磷都没有燃烧的原因分别是 ①:温度未达到红磷的着火点 ②:热水中的白磷没有与氧气(或空气)接触 |
改进后的装置比较,优点是能防止白磷燃烧产生的五氧化二磷逸散,危害人体健康
(3)根据白磷着火点低的性质,同学们进一步思考,将测定空气中氧气含量的实验装置改进如图4所示,经过测量,发现空气中氧气含量不足五分之一,可能的原因是红磷的量不足或是装置的气密性不好都会导致集气瓶内的水位上升不足五分之一.
14.下列化学方程式书写完全正确的是( )
| A. | 4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | B. | 2Fe+6HCl═2FeCl3+3H2↑ | ||
| C. | Cu+FeSO4═CuSO4+Fe | D. | Cu+2AgNO3═Cu(NO3)2+2Ag |
15.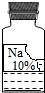 实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小强和小华同学很感兴趣,决定对其成分进行探究:
实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小强和小华同学很感兴趣,决定对其成分进行探究:
【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,这瓶试剂不可能是A.
A.酸 B.碱 C盐
查阅资料】
I.初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3.
Ⅱ.Na2CO3和NaHCO3溶液都呈碱性.
Ⅲ.测定室温(20℃)时,四种物质的溶解度的数据如下:
【得出结论】小华根据试剂瓶标注的溶质质量分数10%和上表中的溶解度的数据判断,这瓶试剂不可能是NaHCO3.
【作出猜想】①可能是NaOH溶液;②可能是Na2CO3溶液;③可能是NaCl.
【设计并实验】
(1)小强用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得pH>7.这瓶试剂不可能是③.
(2)小强为了检验该溶液是NaOH溶液还是Na2C03溶液,他又进行了如下实验:
 实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小强和小华同学很感兴趣,决定对其成分进行探究:
实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小强和小华同学很感兴趣,决定对其成分进行探究:【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,这瓶试剂不可能是A.
A.酸 B.碱 C盐
查阅资料】
I.初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3.
Ⅱ.Na2CO3和NaHCO3溶液都呈碱性.
Ⅲ.测定室温(20℃)时,四种物质的溶解度的数据如下:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度/g | 36 | 109 | 215 | 9.6 |
【作出猜想】①可能是NaOH溶液;②可能是Na2CO3溶液;③可能是NaCl.
【设计并实验】
(1)小强用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得pH>7.这瓶试剂不可能是③.
(2)小强为了检验该溶液是NaOH溶液还是Na2C03溶液,他又进行了如下实验:
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中加 氢氧化钙溶液 | 稀盐酸 | 猜想②正确,相关的化学方程式: Na2CO3+2HCl=2NaCl+H2O+CO2↑ |