题目内容
7.下列实验方案设计合理的是( )| A. | 证明稀盐酸和氢氧化钠溶液发生反应,应向少量混合后的溶液中滴加硝酸银溶液 | |
| B. | 证明二氧化碳和氢氧化钠溶液发生反应,应向少量通入气体后的溶液中滴加稀盐酸 | |
| C. | 证明生石灰中混有熟石灰,应向少量样品中加入水,过滤后向滤液中滴加酚酞溶液 | |
| D. | 证明二氧化碳中混有一氧化碳,应将混合气体通入澄清石灰水 |
分析 A、根据氯离子和硝酸银会生成氯化银沉淀进行分析;
B、根据二氧化碳和氢氧化钠反应会生成碳酸钠,碳酸钠和盐酸反应会生成气体进行分析;
C、根据氧化钙和水反应会生成氢氧化钙进行分析;
D、根据二氧化碳和氢氧化钙反应生成碳酸钙沉淀进行分析.
解答 解:A、氯离子和硝酸银会生成氯化银沉淀,盐酸和氢氧化钠反应生成的氯化钠也含有氯离子,不能验证,故A错误;
B、二氧化碳和氢氧化钠反应会生成碳酸钠,碳酸钠和盐酸反应有气泡产生,可以验证,故B正确;
C、氧化钙和水反应会生成氢氧化钙,不能验证,故C错误;
D、二氧化碳和氢氧化钙反应生成碳酸钙沉淀,不能验证二氧化碳中混有一氧化碳,故D错误.
故选:B.
点评 本题难度不大,但综合性较强,化学实验方案的设计是考查学生能力的主要类型,同时也是实验教与学难点,在具体设计时要对其原理透彻理解,可根据物质的性质结合实验目的进行分析判断.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
17.如图是物质A、B、C的溶解度曲线,下列相关说法正确的是( )
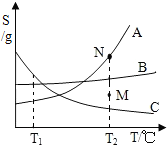

| A. | 若要将B从溶液中结晶出来常采用的方法是降温结晶 | |
| B. | 将T2℃时A、B、C的饱和溶液冷却到T1℃,A溶液的溶质质量分数最小 | |
| C. | 若要将组成在M点的A溶液转变为N点的溶液,只能采取恒温蒸发溶剂的方法 | |
| D. | 将T2℃时组成在M点的C与水的混合物降温至T1℃时,可能得到C的不饱和溶液 |
18.我国科学家用滤纸和二氧化钛(TiO2)薄膜制作出一种新型“纳米纸”,又在纳米纸上“铺”一层“萘胺”(C10H9N)染料制成试纸,用于检测食品中亚硝酸盐浓度的高低.下列说法正确的是( )
| A. | 萘胺中碳元素、氢元素和氮元素的质量比为10:9:1 | |
| B. | 萘胺由10个碳原子、9个氢原子、1个氮原子构成 | |
| C. | 二氧化钛和萘胺都属于氧化物 | |
| D. | 萘胺的相对分子质量为143 |
2.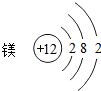 依据如图的原子结构示意图,下列说法正确的是( )
依据如图的原子结构示意图,下列说法正确的是( )
 依据如图的原子结构示意图,下列说法正确的是( )
依据如图的原子结构示意图,下列说法正确的是( )| A. | 该原子的核电荷数为12 | B. | 该原子核外有两个电子 | ||
| C. | 该原子在反应中易得到电子 | D. | 该原子在反应中容易成为阴离子 |
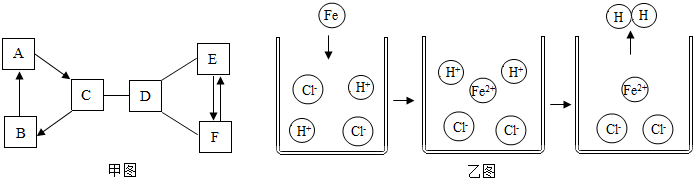
12.金属的应用与其性质密切相关.在“金属与盐溶液反应”的探究课上,同学们将硝酸银溶液倒入装有铜粉的试管中,充分反应后观察到的铜的表面析出银白色物质以及溶液由无色变成蓝色,发生反应的化学方程式为Cu+2AgNO3=Cu(NO3)2+2Ag.过滤后,得到滤渣和滤液.同学们进行了如下探究.
【提出问题】:滤液中溶质的成分是什么?
【猜想与假设】:猜想一:硝酸铜 猜想二:硝酸银和硝酸铜.
【进行实验】:
【解释与结论】:根据对滤液成分的分析,可以推断出滤渣可能的成分是②③(填序号,下同)
①铜 ②银 ③铜和银
【拓展与延伸】:对滤渣回收后,老师要求将滤液中较多的铜离子除去后再排放,以减少对环境的污染.同学们可以向滤液中加入适量的①③.
①铁 ②稀硫酸 ③氢氧化钠溶液 ④氧化钠溶液.
【提出问题】:滤液中溶质的成分是什么?
【猜想与假设】:猜想一:硝酸铜 猜想二:硝酸银和硝酸铜.
【进行实验】:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,向其中滴入稀盐酸 | 无明显现象 | 猜想一正确 |
①铜 ②银 ③铜和银
【拓展与延伸】:对滤渣回收后,老师要求将滤液中较多的铜离子除去后再排放,以减少对环境的污染.同学们可以向滤液中加入适量的①③.
①铁 ②稀硫酸 ③氢氧化钠溶液 ④氧化钠溶液.
19.工业上通过以下反应将二氧化硅(SiO2)转化为硅:SiO2+2C $\frac{\underline{\;高温\;}}{\;}$ Si+2CO↑,该反应属于( )
| A. | 置换反应 | B. | 分解反应 | C. | 复分解反应 | D. | 化合反应 |