题目内容
聚合硫酸铁是一种新型水处理剂,其化学组成为Fex(OH)y(SO4)z?nH2O.取7.525g样品溶于水,加入过量的BaCl2溶液得到10.485g BaSO4沉淀.再向滤液中加入适量碱,经过滤、洗涤、灼烧得Fe2O3固体2.80g.下列关系正确的是( )
| A、x:y=7:3 |
| B、2x=y+2z |
| C、y:z=1:3 |
| D、3x=2y+2z |
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:依据反应前后硫酸根和铁的微粒个数相同对该物质的化学式进行分析解答即可;
解答:解:10.48gBaSO4 中硫酸根的物质的量是 0.045 mol,Fe2O3固体2.8g 则该固体中铁的物质的量是 0.035 mol,由于是+3价铁,所以电荷就是 0.035×3=0.105mol;硫酸根提供的负电荷是 0.045×2=0.090mol,所以OH根提供的电荷就是 0.105mol-0.090mol=0.015mol,对应的OH根就是 0.015 mol.于是有分子式 Fe35(OH)15(SO4)45,化简得到 Fe7(OH)3(SO4)9.x:y:z=7:3:9;
故选:AC;
故选:AC;
点评:本题是一道计算知识的题目,考查学生分析和解决问题的能力,综合性较强,难度大,解题的关键是利用元素的质量守恒分析解答.

练习册系列答案
相关题目
实验室用高锰酸钾制氧气时,不需要用到的仪器是( )
| A、量筒 | B、单孔橡皮塞 |
| C、酒精灯 | D、药匙 |
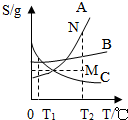 如图是物质A、B、C的溶解度曲线.下列相关说法正确的是( )
如图是物质A、B、C的溶解度曲线.下列相关说法正确的是( )| A、若要将B从溶液中结晶出来,常采用降温结晶的方法 |
| B、A的溶解度比B大 |
| C、T2℃时,组成在M点的A溶液为饱和溶液 |
| D、将T2℃时,C的饱和溶液降温至T1℃,则变为C的不饱和溶液(原溶液中无固体) |
已知氢气、一氧化碳、二氧化碳混合气体共20g,其中含碳元素质量为40%,将混合气体通入足量的氧化铜,再通入足量的石灰水,最后得到沉淀的质量可能是( )
| A、66.7g |
| B、30 g |
| C、100g |
| D、12 |
 甲、乙两种物质的溶解度曲线如图所示,下列说法中正确的是( )
甲、乙两种物质的溶解度曲线如图所示,下列说法中正确的是( )| A、30℃时,50 g水可以溶解25g甲物质 |
| B、升温能使甲物质的不饱和溶液变为饱和溶液 |
| C、20℃时,分别在100g水中加入15g甲、乙,完全溶解后所得溶液中溶质的质量分数相等 |
| D、甲、乙两种物质的饱和溶液由30℃降温到20℃后,甲析出晶体,乙不析出晶体,甲溶液中溶质的质量分数大于乙溶液中溶质的质量分数 |
在反应X+2Y═R+2M中,已知R和M的相对分子质量之比为2:9,当1.6g X和Y完全反应后,生成4.4g R.则在反应中,Y与M的质量比为( )
| A、106:99 | B、23:9 |
| C、32:9 | D、46:9 |
下列关于燃烧现象的描述,正确的是( )
| A、碳在氧气中燃烧生成二氧化碳 |
| B、红磷在空气中燃烧产生大量白色烟雾 |
| C、氢气在空气中燃烧产生淡蓝色火焰 |
| D、铁丝在空气中剧烈燃烧,火星四射 |
下列能由相应金属和酸直接反应得到的物质是( )
| A、AgCl |
| B、ZnSO4 |
| C、FeCl3 |
| D、CuSO4 |
6.5g含杂质的锌粉和足量的稀硫酸反应,生成0.21g氢气,则锌粉中含有的杂质可能是( )
| A、Ag | B、Cu | C、Mg | D、Zn |