题目内容
6.乙醇(C2H5OH)俗称酒精,是化学实验室常用的燃料和有机溶剂,请计算:(1)乙醇中氢元素和氧元素的质量比为3:8;
(2)乙醇中碳元素的质量分数为52.2%(计算结果精确到0.1%).
分析 根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
根据化合物中元素的质量分数计算公式进行分析解答.
解答 解:(1)乙醇中氢、氧元素的质量比=(1×6):(16×1)=3:8.
(2)乙醇中碳元素的质量分数=$\frac{12×2}{12×2+1×6+16×1}$×100%≈52.2%.
故答案为:(1)3:8;(2)52.2%.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算的能力.

练习册系列答案
相关题目
16.如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
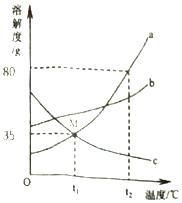

| A. | M点表示a、c两种物质的饱和溶液质量相等 | |
| B. | t1℃时,b物质的饱和溶液升温至t2℃时仍是饱和溶液 | |
| C. | 将t1℃时三种物质的饱和溶液升温到t2℃时,所得溶液中溶质的质量分数的大小关系是:b>a=c | |
| D. | t1℃时,a物质的饱和溶液中溶质和溶剂的质量比为7:20 |
14.下列事故的处理方法正确的是( )
| A. | 家庭厨房发现有煤气泄漏,立即开灯查找泄漏点 | |
| B. | 发生一氧化碳中毒,立即转移到通风的地方救治 | |
| C. | 电器着火时,立即用泡沫灭火器灭火 | |
| D. | 室内失火时,立即打开所有门窗 |
11.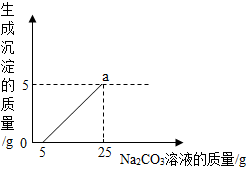 石灰石是主要修路材料之一,某兴趣小组用修路材料石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,该小组取石灰石20g,将一定质量的稀盐酸平均分5次加入其中,记录数据如下:
石灰石是主要修路材料之一,某兴趣小组用修路材料石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,该小组取石灰石20g,将一定质量的稀盐酸平均分5次加入其中,记录数据如下:
在准备将反应后的废液倒进废液缸时,发现实验桌上有一拼未知质量分数的Na2CO3溶液,他们决定利用该废液,测定这瓶Na2CO3溶液中溶质的质量分数.他们将废液过滤,取部分溶液的质量与生产沉淀质量的关系如图所示.请计算:
(1)表中m=13.4;
(2)当20g石灰石完全反应时生成CO2的质量;
(3)Na2CO3溶液中溶质的质量分数和a点时溶液中溶质的质量.
 石灰石是主要修路材料之一,某兴趣小组用修路材料石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,该小组取石灰石20g,将一定质量的稀盐酸平均分5次加入其中,记录数据如下:
石灰石是主要修路材料之一,某兴趣小组用修路材料石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,该小组取石灰石20g,将一定质量的稀盐酸平均分5次加入其中,记录数据如下:| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 剩余固体的质量/g | 17.8 | 15.6 | 13.4 | m | 13.4 |
(1)表中m=13.4;
(2)当20g石灰石完全反应时生成CO2的质量;
(3)Na2CO3溶液中溶质的质量分数和a点时溶液中溶质的质量.
15.2017“地球一小时”全球主题是“气候、人类、社会”,倡导健康安全的生活理念,下列说法不合理的是( )
| A. | 奶制品中含钙丰富,是日常饮食中钙的来源之一 | |
| B. | 食物合理搭配,以保证各种营养素的均衡摄入 | |
| C. | 硒、碘等微里元素在人体中的含量很小,对维持正常生命活动作用不大 | |
| D. | 糖类和油脂在人体内经氧化释放能量,提供机体活动和维持恒定体温的需要 |
15.最近,“镉大米”成为公众关注的热点问题之一.据了解,含镉的大米对人的肝肾损害比较大.镉大米中的“镉”是指( )
| A. | 原子 | B. | 分子 | C. | 元素 | D. | 单质 |
 空调是常见的家用电器,如图为空调的实物图
空调是常见的家用电器,如图为空调的实物图