题目内容
甲、乙两同学用氧化铜做了如下的实验,请回答有关问题:甲同学:取40g氧化铜与足量的稀硫酸充分反应后得到蓝色溶液.
(1)甲同学所得溶液显蓝色的溶质的化学式为______.
(2)溶液中含硫酸铜的质量是多少?写出计算过程.
乙同学:将五份含6g碳粉和40g的氧化铜的混合物,分别放入密闭容器中隔绝空气加强热.在不同的反应时间里收集到如下数据:
| 加热时间/min | 2 | 4 | 6 | 8 | 10 |
| 固体质量/g | 44 | 39 | 35 | 32 | 32 |
| 气体质量/g | X | 7 | 11 | 14 | 14 |
②混合固体在加热过程中发生的反应有:
CuO+C
 Cu+CO↑、2CuO+C
Cu+CO↑、2CuO+C 2Cu+CO2↑,还可能发生反应的化学方程式为______ 2CO
2Cu+CO2↑,还可能发生反应的化学方程式为______ 2CO
【答案】分析:(1)根据氧化铜与硫酸反应的生成物考虑;(2)根据氧化铜的质量算出硫酸铜的质量;(3)①根据固体质量的减少量与气体的增加量的关系考虑;②根据碳与二氧化碳的反应考虑;根据加热8min后容器内的气体变化,考虑生成物.
解答:解:(1)氧化铜与硫酸反应,生成硫酸铜和水,硫酸铜溶液是蓝色;
(2)设40g氧化铜与硫酸反应生成硫酸铜的质量为X则:
CuO+H2SO4=CuSO4+H2O
80 160
40g X
根据: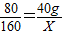 解得X=80g;
解得X=80g;
(3)①在4min和6min之间固体质量减少了39-35=4,气体质量增加了11-7=4;在6min和8min之间固体减少了35-32=3,气体质量增加了14-11=3,所以固体质量的减少量,正好等于气体的增加量,加热2min固体质量减少了:46-44=2,所以收集到气体的质量是2g;
②假设此反应中碳粉足量,算出完全反应时,生成CO2的质量为11g,符合题意;假设此反应中CuO足量,算出完全反应时,生成CO2的质量为22g,不符合题意.综上所述,此反应中一定是碳粉足量.然后,算出此时,生成Cu的质量恰为32g,说明过量的碳粉一定全部转化为了气体,据此算出先前参与反应的碳粉质量为3g,故碳粉剩余3g,而它们恰好能与11gCO2完全反应,生成14gCO,故得出结论:此时容器内的气体一定全部是CO
点评:解答本题关键是要知道根据图表中数据分析出固体质量的减少量,正好等于气体的增加量,再进一步进行分析即可.
解答:解:(1)氧化铜与硫酸反应,生成硫酸铜和水,硫酸铜溶液是蓝色;
(2)设40g氧化铜与硫酸反应生成硫酸铜的质量为X则:
CuO+H2SO4=CuSO4+H2O
80 160
40g X
根据:
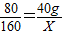 解得X=80g;
解得X=80g;(3)①在4min和6min之间固体质量减少了39-35=4,气体质量增加了11-7=4;在6min和8min之间固体减少了35-32=3,气体质量增加了14-11=3,所以固体质量的减少量,正好等于气体的增加量,加热2min固体质量减少了:46-44=2,所以收集到气体的质量是2g;
②假设此反应中碳粉足量,算出完全反应时,生成CO2的质量为11g,符合题意;假设此反应中CuO足量,算出完全反应时,生成CO2的质量为22g,不符合题意.综上所述,此反应中一定是碳粉足量.然后,算出此时,生成Cu的质量恰为32g,说明过量的碳粉一定全部转化为了气体,据此算出先前参与反应的碳粉质量为3g,故碳粉剩余3g,而它们恰好能与11gCO2完全反应,生成14gCO,故得出结论:此时容器内的气体一定全部是CO
点评:解答本题关键是要知道根据图表中数据分析出固体质量的减少量,正好等于气体的增加量,再进一步进行分析即可.

练习册系列答案
相关题目
甲、乙两同学用氧化铜做了如下实验,请回答有关问题:
甲同学:向100g19.6%的稀硫酸中加入氧化铜至不再继续溶解.
(1)反应结束后观察到所得溶液为______色.
(2)反应结束后溶液中含硫酸铜的质量是多少?写出计算过程.
乙同学:将五份含6g炭粉和40g氧化铜的混合物,分别放入密闭的容器中隔绝空气加强热.在不同的反应时间里收集到如下数据:
| 加热时间/min | 2 | 4 | 6 | 8 | 10 |
| 固体质量/g | 44 | 39 | 35 | 32 | 32 |
| 气体质量/g | 2 | 7 | 11 | 14 | X |
(2)混合固体在加热过程中产生的反应有:CuO+C
 Cu+CO↑、2CuO+C
Cu+CO↑、2CuO+C 2Cu+CO2↑,将炭粉和氧化铜按照下列质量比混合后进行上述实验,所得气体为CO和CO2的是______(填序号).
2Cu+CO2↑,将炭粉和氧化铜按照下列质量比混合后进行上述实验,所得气体为CO和CO2的是______(填序号).A、3:40 B、3:35 C、3:25 D、3:20.
甲、乙两同学用氧化铜做了如下实验,请回答有关问题:
甲同学:向100g19.6%的稀硫酸中加入氧化铜至不再继续溶解.
(1)反应结束后观察到所得溶液为______色.
(2)反应结束后溶液中含硫酸铜的质量是多少?写出计算过程.
乙同学:将五份含6g炭粉和40g氧化铜的混合物,分别放入密闭的容器中隔绝空气加强热.在不同的反应时间里收集到如下数据:
(1)加热10min收集到气体的质量是______g.
(2)混合固体在加热过程中产生的反应有:CuO+C Cu+CO↑、2CuO+C
Cu+CO↑、2CuO+C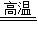 2Cu+CO2↑,将炭粉和氧化铜按照下列质量比混合后进行上述实验,所得气体为CO和CO2的是______(填序号).
2Cu+CO2↑,将炭粉和氧化铜按照下列质量比混合后进行上述实验,所得气体为CO和CO2的是______(填序号).
A、3:40 B、3:35 C、3:25 D、3:20.
甲同学:向100g19.6%的稀硫酸中加入氧化铜至不再继续溶解.
(1)反应结束后观察到所得溶液为______色.
(2)反应结束后溶液中含硫酸铜的质量是多少?写出计算过程.
乙同学:将五份含6g炭粉和40g氧化铜的混合物,分别放入密闭的容器中隔绝空气加强热.在不同的反应时间里收集到如下数据:
| 加热时间/min | 2 | 4 | 6 | 8 | 10 |
| 固体质量/g | 44 | 39 | 35 | 32 | 32 |
| 气体质量/g | 2 | 7 | 11 | 14 | X |
(2)混合固体在加热过程中产生的反应有:CuO+C
 Cu+CO↑、2CuO+C
Cu+CO↑、2CuO+C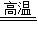 2Cu+CO2↑,将炭粉和氧化铜按照下列质量比混合后进行上述实验,所得气体为CO和CO2的是______(填序号).
2Cu+CO2↑,将炭粉和氧化铜按照下列质量比混合后进行上述实验,所得气体为CO和CO2的是______(填序号).A、3:40 B、3:35 C、3:25 D、3:20.