题目内容
1.除去下列物质中的少量杂质,所用试剂及操作方法均正确的是( )| 选项 | 物质(括号内为杂质) | 所用试剂及操作方法 |
| A | FeSO4(CuSO4) | 加入足量的水,加入足量的铁粉,过滤,蒸发结晶 |
| B | NaOH溶液(Na2CO3) | 加入适量氢氧化钙溶液,过滤 |
| C | 铜粉(氧化铁粉末) | 加入足量稀盐酸,过滤,洗涤,干燥 |
| D | N2(O2) | 将气体通过灼热的炭层 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、足量的铁粉能与CuSO4溶液反应生成硫酸亚铁溶液和铜,但应先加水溶解,再加入铁粉,故选项所采取的方法错误.
B、Na2CO3能与适量氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠,再进行过滤,故选项所采取的方法正确.
C、氧化铁粉末能与足量稀盐酸反应生成氯化铁和水,铜能与氯化铁反应生成氯化铜和氯化亚铁溶液,故选项所采取的方法错误.
D、灼热的炭层能与O2反应生成二氧化碳气体,能除去杂质但引入了新的杂质二氧化碳,不符合除杂原则,故选项所采取的方法错误.
故选:B.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
相关题目
8.生活中的下列四种物品,都用到的材料是( )


| A. | 金属材料 | B. | 天然纤维 | C. | 合成材料 | D. | 玻璃制品 |
9.下列说法中,错误的是( )
| A. | 动、植物体内,都含有大量的水 | |
| B. | 凡是无色透明的水都能喝 | |
| C. | 水在日常生活中和工农业生产上,都有重要作用 | |
| D. | 水资源是无穷无尽的 |
9.钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量.某补钙药剂说明书的部分信息如图1所示.现将125g盐酸分成5等份,逐次加到用50片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图象如下.请根据有关信息回答问题.
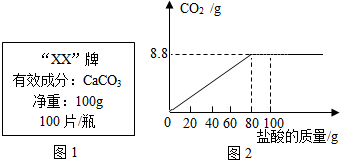
(1)该品牌补钙药剂中CaCO3的质量分数是40%,a的数值为35.
(2)求该盐酸中溶质的质量分数(写出计算过程,计算结果保留一位小数).
(3)求恰好完全反应时所得溶液的溶质质量分数(写出计算过程,计算结果保留一位小数).

| 第1次 | 第3次 | 第4次 | |
| 加入盐酸的质量(g) | 25 | 25 | 25 |
| 剩余固体的质量(g) | 45 | a | 30 |
(2)求该盐酸中溶质的质量分数(写出计算过程,计算结果保留一位小数).
(3)求恰好完全反应时所得溶液的溶质质量分数(写出计算过程,计算结果保留一位小数).
16.甲、乙两个小组对蜡烛燃烧分别进行了如下探究,请完成下列实验报告.
(一)甲组同学实验:
(二)乙组同学对蜡烛燃烧进行了如下拓展实验:
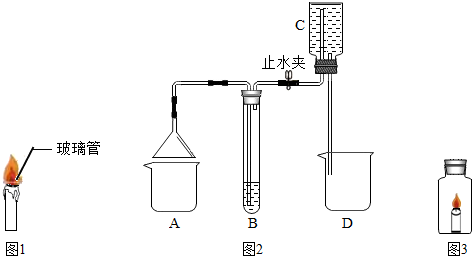
(1)向焰心斜向插入一直细玻璃管(如图1所示),发现玻璃管中无明显现象,在玻璃管的上口点燃,上口产生火焰,这说明焰心处物质的性质有该气体具有可燃性,可以燃烧(写2条).
(2)该小组同学用图2所示装置检验蜡烛燃烧后的气体,在A处烧杯中放置燃烧的蜡烛,打开止水夹,观察到B中无色溶液变浑浊.蜡烛燃烧产生的气体能被吸入B中的原因是C中水流入D中,使装置中气体压强减小,生成的气体被吸入B中.
(3)蜡烛(足量)在如图3密闭装置内燃烧至熄灭,用仪器测出这一过程中瓶内氧气体积分数的变化如图所示,下列判断正确的是B(填字母序号).
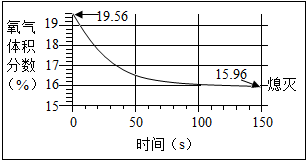
A.蜡烛燃烧前装置内只有氧气
B.氧气浓度小于一定值时,蜡烛无法燃烧
C.蜡烛熄灭后瓶内只剩二氧化碳气体.
(一)甲组同学实验:
| 实验序号 | 实验操作 | 实验现象 | 实验分析及结论 |
| 实验1 点燃前  | 用指甲在蜡烛上进行刻划 | 蜡烛上留下很多划痕 | 说明蜡烛质软 |
| 实验2 燃烧时  | 在蜡烛火焰上方罩一个干冷的烧杯 | 烧杯内壁有水雾生成 | 说明蜡烛燃烧生成了H2O,同时放出热量 |
| 在蜡烛火焰上方罩 的烧杯 | 澄清石灰水变浑浊 | 说明蜡烛燃烧生成了CO2 | |
| 实验3 熄灭后  | 吹灭蜡烛 | 自烛芯出产生一缕白烟 | 白烟的主要成分是石蜡蒸气遇冷凝成的石蜡小颗粒 |
| 用火柴点燃白烟 | 蜡烛能重新燃烧 |

(1)向焰心斜向插入一直细玻璃管(如图1所示),发现玻璃管中无明显现象,在玻璃管的上口点燃,上口产生火焰,这说明焰心处物质的性质有该气体具有可燃性,可以燃烧(写2条).
(2)该小组同学用图2所示装置检验蜡烛燃烧后的气体,在A处烧杯中放置燃烧的蜡烛,打开止水夹,观察到B中无色溶液变浑浊.蜡烛燃烧产生的气体能被吸入B中的原因是C中水流入D中,使装置中气体压强减小,生成的气体被吸入B中.
(3)蜡烛(足量)在如图3密闭装置内燃烧至熄灭,用仪器测出这一过程中瓶内氧气体积分数的变化如图所示,下列判断正确的是B(填字母序号).

A.蜡烛燃烧前装置内只有氧气
B.氧气浓度小于一定值时,蜡烛无法燃烧
C.蜡烛熄灭后瓶内只剩二氧化碳气体.
6.下列用品有效成分的化学式及用途对应正确的是 ( )
| A、小苏打 | B、硝酸钾 | C、葡萄糖 | D、烧碱 | |
| 用品 |  |  |  |  |
| 有效成分 | Na2CO3 | KNO3 | C6H12O6 | NaOH |
| 用途 | 做发酵粉 | 做复合肥 | 做调味剂 | 治疗胃酸过多 |
| A. | A | B. | B | C. | C | D. | D |
13.从化学的视角看食品添加剂,主要是从其元素组成与结构、物理化学性能及在人体内的变化等方面来研究.结合表中信息回答下列问题.
(1)国家严格禁止甲醛作为食品添加剂的原因是甲醛是有毒物质,对人体有害或有毒,能使人体中蛋白质失去生理活性.
(2)还原性铁粉用于食品添加剂,除能够防止食品因氧化而变质外,还是一种营养强化剂,这是因为Fe+2HCl═FeCl2+H2↑.(用化学方程式表示)
(3)甜蜜素与蔗糖一样都能给食物提供甜味,但是甜蜜素不能(填“能”或“不能”)为人体提供能量.
(4)碳酸氢钠是发酵粉的主要成分,在制作面包、饼干、糕点时人们常常加适量的碳酸氢钠,其作用是2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.(用化学方程式表示)
(5)亚硝酸钠(NaNO2)外观酷似食盐,有咸味,常被误作食盐食用而导致中毒事件发生.有一包外观酷似食盐的固体,结合表中信息,如何鉴别它是亚硝酸钠还是氯化钠?取样,溶于水,加入硝酸银溶液,产生白色沉淀的是氯化钠,产生黄色沉淀的是亚硝酸钠(包括选取的试剂、方法、实验现象和结论,只写出一种方法即可).
(6)食品添加剂能改善食品的色香味、延长食品的保质期、提高食品的品质,但副作用也是显而易见的.结合食品添加剂谈一下你对化学的认识合理利用化学物质可以造福于人类,反之则会给人类带来危害.
| 物质的组成与性能 | 用于食品添加剂 | |||
| 物质名称 | 物质组成 | 主要化学性质及在体内变化 | 类别或作用 | 法律规定 |
| 碳酸氢钠 | NaHCO3 | 无毒、弱碱性,易与胃酸反应,加热分解成碳酸钠、水和二氧化碳 | 膨松剂 | 可用 |
| 铁 (还原性铁粉) | Fe | 比较活泼的金属,能与胃酸反应 | 抗氧化剂 | 依据国家标准可用 |
| 甜蜜素 | C4H12NSO2Na | 白色结晶状粉末,味甜,甜度为蔗糖的40~50倍,为无营养甜味剂 | 调味剂 | 依据国家标准可用 |
| 甲醛 | CH2O | 防腐 | 国家严禁使用 | |
| 亚硝酸钠 | NaNO2 | 易溶、水溶液显碱性,跟硝酸银反应生成浅黄色沉淀 | 发色剂、防腐剂 | 严格依据国家标准 |
(2)还原性铁粉用于食品添加剂,除能够防止食品因氧化而变质外,还是一种营养强化剂,这是因为Fe+2HCl═FeCl2+H2↑.(用化学方程式表示)
(3)甜蜜素与蔗糖一样都能给食物提供甜味,但是甜蜜素不能(填“能”或“不能”)为人体提供能量.
(4)碳酸氢钠是发酵粉的主要成分,在制作面包、饼干、糕点时人们常常加适量的碳酸氢钠,其作用是2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.(用化学方程式表示)
(5)亚硝酸钠(NaNO2)外观酷似食盐,有咸味,常被误作食盐食用而导致中毒事件发生.有一包外观酷似食盐的固体,结合表中信息,如何鉴别它是亚硝酸钠还是氯化钠?取样,溶于水,加入硝酸银溶液,产生白色沉淀的是氯化钠,产生黄色沉淀的是亚硝酸钠(包括选取的试剂、方法、实验现象和结论,只写出一种方法即可).
(6)食品添加剂能改善食品的色香味、延长食品的保质期、提高食品的品质,但副作用也是显而易见的.结合食品添加剂谈一下你对化学的认识合理利用化学物质可以造福于人类,反之则会给人类带来危害.
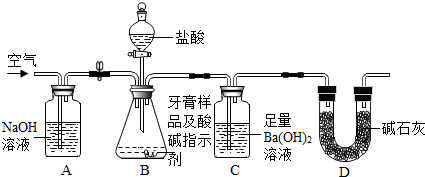
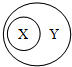 下列选项符合图示从属关系的是( )
下列选项符合图示从属关系的是( )